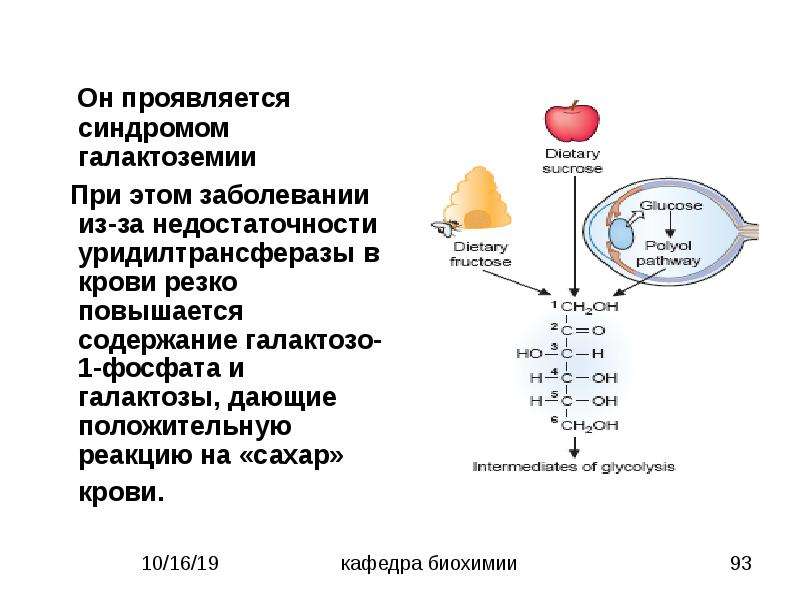
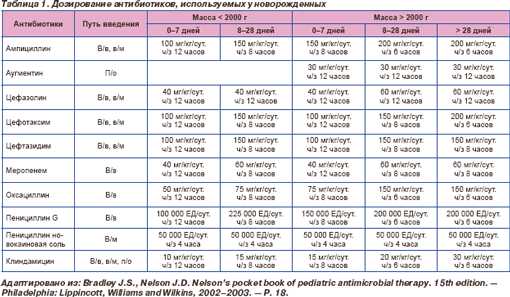
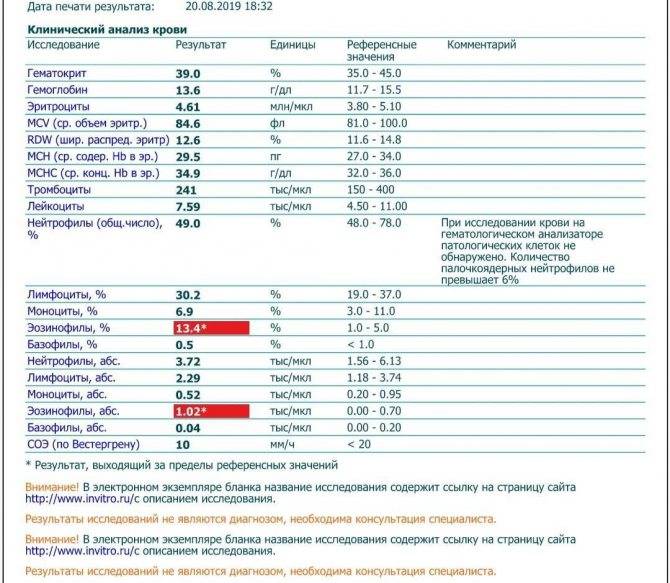
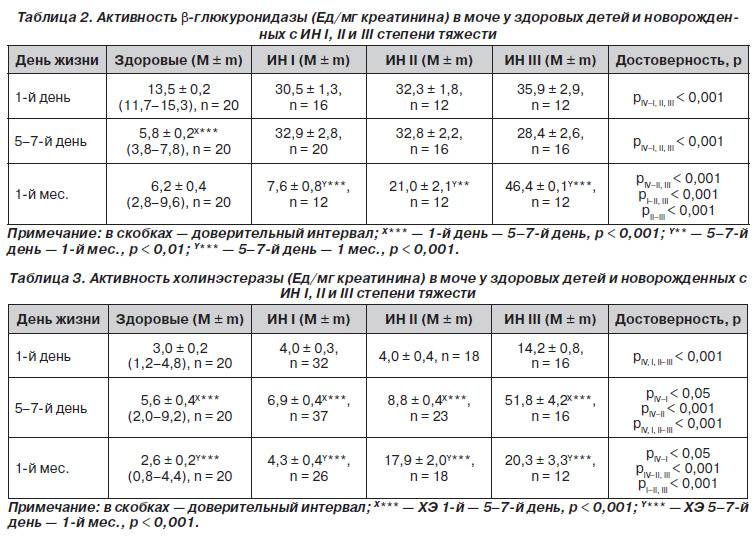
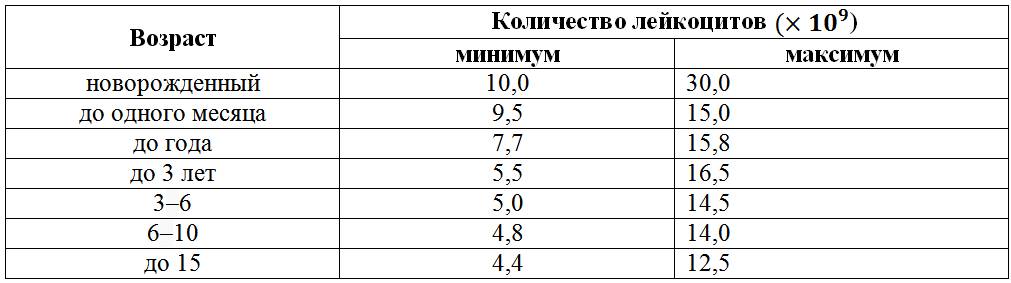
Чем опасно снижение уровня глюкозы?
Гипогликемия особенно опасна для детей, рожденных раньше срока. Чем меньше плод находится в утробе матери, тем менее приспособленным к окружающей среде он является и тем большему риску развития различных патологий он подвержен.
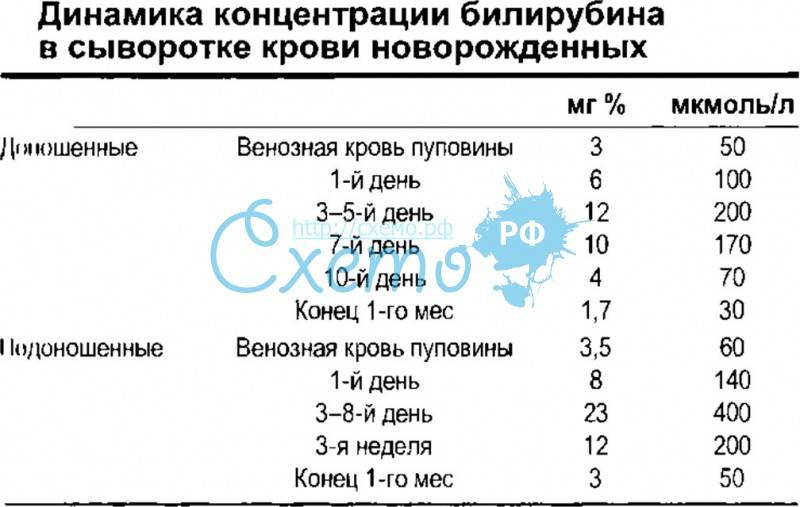
Низкое значение глюкозы в крови – показатель не только гипогликемии, он может свидетельствовать о других нарушениях работы организма. Беспокойство должен вызывать уровень сахара ниже 2,2 ммоль/л. Это патологическое состояние часто становится причиной смерти новорожденных, т.к. дети с выраженной гипогликемией не выживают во время родов.

Подготовка к анализу
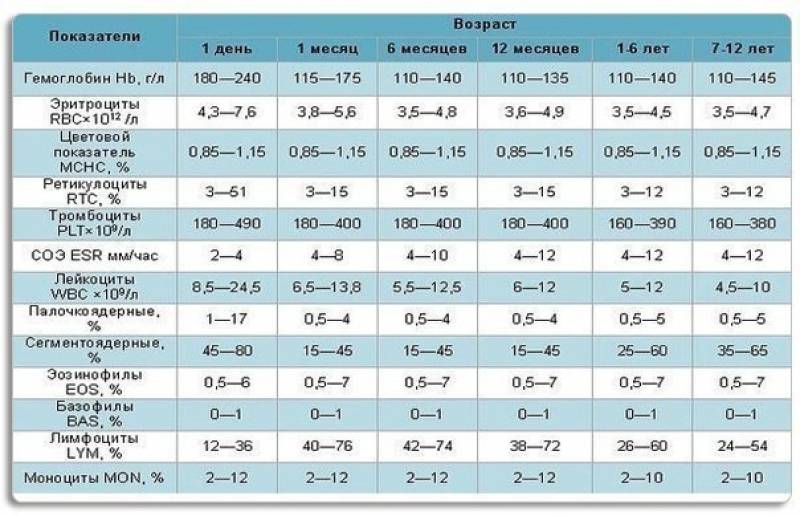
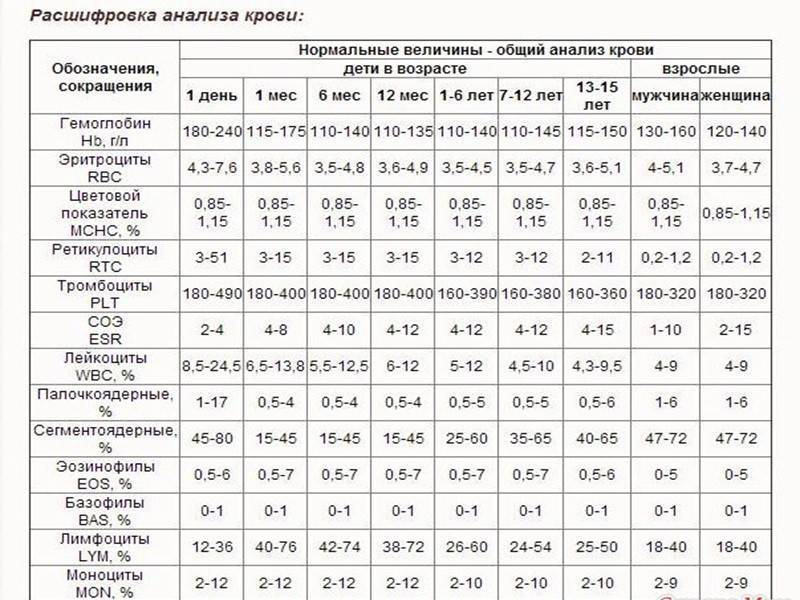
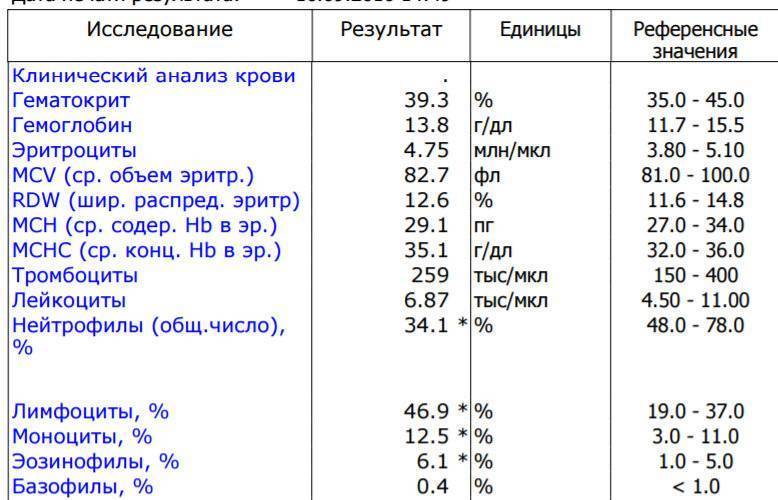
Прямые анализы на mchc не делаются, для вычисления используют данные общего анализа (ОАК). Для его проведения кровь берется из вены, количество – до 3 мл. При наличии определенных показателей возможно взятие капиллярной крови, такой анализ назначают детям в возрасте до 3 лет, больным с патологиями свертывающей системы крови.
Особой подготовки к общему анализу крови не требуется. Забор крови выполняется утром, натощак, либо в любое удобное время суток. Главное условие – не принимать пищу на протяжении минимум 8 часов перед анализом. Можно пить воду, но не кофе, чай либо сладкие напитки.
Для повышения достоверности полученных данных за 1-2 суток до взятия крови рекомендуется избегать стрессов, чрезмерных физических и психоэмоциональных нагрузок. Стоит избегать употребления алкоголя.
От чего зависит сохранность рН?
Рассмотрим, какие системы отвечают за соблюдение этого постоянства. Эти системы называются буферными системами, поскольку они позволяют или забирать, или отдавать в кровь протоны, без каких-либо резких колебаний pH, тем самым компенсируя возможные метаболические нарушения сразу, по мере их возникновения.
К основным буферным системам организма относятся следующие:
- бикарбонатная система, которая «работает» на угольной кислоте и ее соли – бикарбонате натрия,
- гемоглобиновая буферная система, использующая белки.
В том случае, когда гемоглобин присоединяет кислород в легких, он проявляет более сильные кислые свойства, а когда гемоглобин отдает кислород в тканях, то его кислотные свойства ослабевают, и он становится акцептором протонов.
Кроме двух буферных систем, поддерживать в норме биохимический анализ крови позволяет дыхание. В течение нескольких минут (2 – 3) лёгкие компенсируют любое физиологическое изменение pH крови, доводя его до нормы. Системам бикарбоната и гемоглобина вследствие высокой буферной емкости для этого нужно всего лишь около половины минуты. Но лёгкие, благодаря выделению во внешнюю среду углекислого газа, быстро ликвидируют опасность закисления внутренней среды организма.
Кроме этого, еще одним важным механизмом является образование мочи. В почках протекает сложный процесс изменения концентрации карбонатного буфера. Почки являются самым медленным, но надежным механизмом: для нормализации показателей кислотности в плазме им требуется около половины суток.
В основном, почки используют обратное всасывание ионов натрия и секрецию протонов в почечных канальцах. Почки являются мощным и эффективным механизмом вывода лишней кислотности из организма. Разница между концентрацией рН в моче и в плазме может достигать соотношения 800: 1.
Для того чтобы определить pH крови, в современной лаборатории достаточно воспользоваться артериальной кровью из капилляров, то есть просто проколоть палец пациенту. Поскольку расшифровка состояния и состава КЩС как взрослого человека, так и ребенка является одним из важнейших показателей гомеостаза, то в анализы входят следующие показатели:
- величина рН,
- напряжение, или парциальное давление углекислого газа в плазме,
- концентрация бикарбоната,
- концентрация буферных оснований,
- избыток оснований.
В клинике существуют различные способы определения этих параметров. Мы не будем подробно останавливаться на тонкостях и особенностях диагностики различных показателей на кислотность, а остановимся на причинах, которые могут привести к изменениям кислотно-щелочного равновесия, связанные с различными заболеваниями, вызванные нарушениями в организме, и превышающими физиологическую норму.
Анализ на непереносимость молока
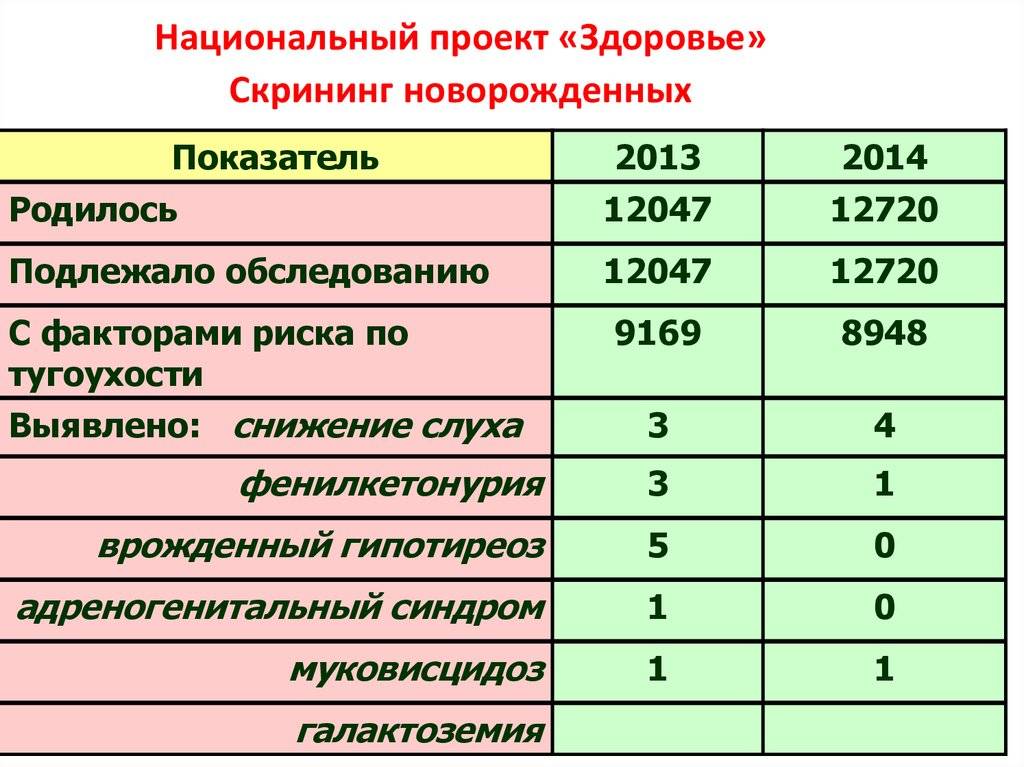
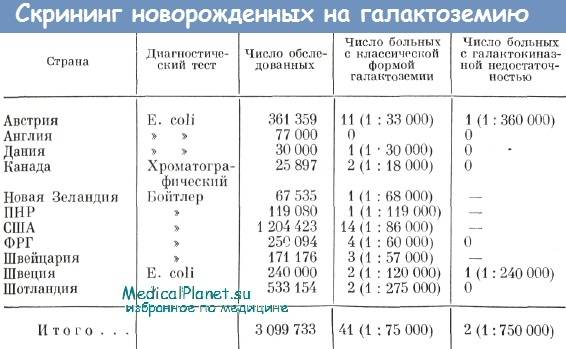
В нашей стране принят закон об обязательном тестировании каждого новорожденного на галактоземию. В первые дни жизни малыша в родильном доме проводится анализ на непереносимость молока для определения уровня галактозы. Если он превышает норму, семью вызывают в медико-генетический центр, где уровень галактозы измеряют повторно. При сохраняющемся повышенном уровне галактозы нужно проводить уточняющую диагностику. Умеренное повышение встречается нередко и характерно для доброкачественного варианта галактоземии, который обычно никак не проявляется клинически.
Непереносимость молока не всегда связана с усвоением молочных сахаров. Если у ребенка после маминого или коровьего молока возникают покраснения и воспаления на коже, то, вероятно, у него аллергия на белок молока.
ДНК-диагностика позволяет отличить классическую галактоземию, при которой требуется срочное назначение безлактозной диеты, от доброкачественного варианта, при котором в большинстве случаев можно сохранить грудное вскармливание, а также от других наследственных болезней обмена, протекающих со сходной симптоматикой.
Еще одна причина обращения к генетическому исследованию – прогноз потомства. Родители ребенка, больного галактоземией, имеют высокий риск рождения второго больного ребенка. Генетическое обследование семьи дает возможность уже на ранних стадиях беременности узнать, будет ли болен будущий ребенок.
При непереносимости молока генетический анализ также позволяет различить первичную и вторичную лактазную недостаточность
Это важно, так как при первичном дефиците лактазы пожизненно назначается низколактозная диета, а при вторичном необходимо устранить основную причину, вызвавшую повреждение кишечника
Что такое лактазная недостаточность?
Врожденная лактазная недостаточность – это очень редкое жизнеугрожающее состояние новорожденного, развивающееся из-за мутаций в гене, кодирующем лактазу. Заболевание проявляется в первые дни жизни ребенка, выявить его поможет специальный анализ ДНК. После кормления грудным молоком возникают срыгивания, кишечные колики и водянистая диарея — это симптомы непереносимости грудного молока у ребенка. Продолжение кормления малыша молоком матери или молочными смесями может приводить к сильному обезвоживанию.
Тяжелые последствия можно предотвратить, переведя новорожденного на безлактозную диету. И хотя, как всем известно, грудное молоко – продукт совершенно уникальный для ребенка, обеспечивающий, в частности, его врожденный иммунитет, в данном случае от него придется отказаться.
Существует также лактазная недостаточность недоношенных детей, при которой активность фермента со временем нормализуется без диеты.
Вторичная непереносимость молока возникает из-за повреждения клеток кишечника, вырабатывающих лактазу, при инфекционном или аллергическом воспалении.
Общие сведения
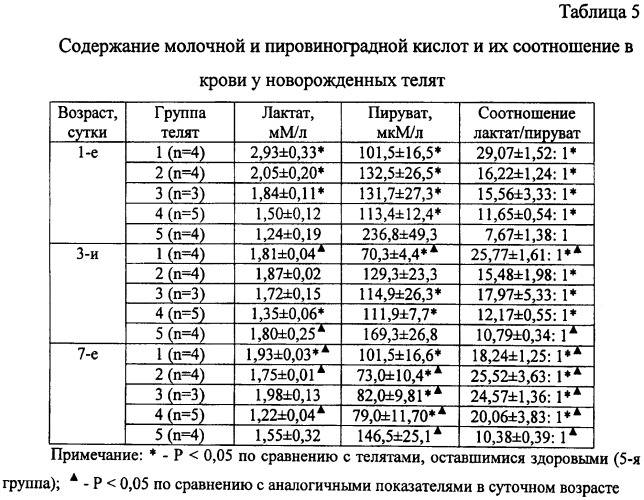
Лактат – это продукт клеточного метаболизма, который может присутствовать в организме в виде молочной кислоты или ее солей (в норме его содержание минимально). Утилизируют лактат печень, почки, сердце, головной мозг. При дефиците кислорода в клетках тканей концентрация молочной кислоты в крови повышается.
При достижении так называемого «лактатного порога», когда внутренние органы не успевают справляться с объемами молочной кислоты, лактат начинает накапливаться в организме (гиперлактатацидемия). Это состояние может перерасти в лактацидоз (закисление), который организм успешно нейтрализует. Но в самых тяжелых случаях происходит нарушение кислотно-щелочного баланса, что проявляется негативной симптоматикой (слабость, учащение дыхания, тошнота, рвота, потливость).
Лактацидоз подразделяется на 2 типа:
Тип А – развивается на фоне замедления кровообращения и недостаточного снабжения клеток тканей кислородом. Лактацидоз А-типа сопровождает следующие заболевания:
- тяжелая анемия;
- отек легких;
- сердечно-сосудистая недостаточность;
- инфаркт миокарда;
- сепсис (общее заражение организма патогенными микроорганизмами);
- шок в результате кровотечения или травмы;
Тип Б – возникает при нарушении метаболизма молочной кислоты. Примеры лактацидоза Б-типа:
- сахарный диабет;
- эпилепсия;
- почечная недостаточность;
- патологии печени;
- онкологические процессы (лейкемия, лимфома);
- СПИД;
- тяжелое отравление алкоголем, салицилатами, цианидом, метанолом и пр.
Также выброс молочной кислоты может дать чрезмерная физическая нагрузка.
Под воздействием накопленного лактата рН крови изменяется в кислую сторону, что является опасным для здоровья и требует эффективного лечения.
Для подтверждения лактатного ацидоза проводят биохимический анализ крови и анализируют 2 компонента: концентрация молочности кислоты в сыворотке, соотношение лактата и пирувата.
Каким анализом определяют уровень глюкозы в крови?
Для проведения анализа, который покажет, что норма глюкозы в крови соответствует принятым у врачей значениям или же, наоборот, отклоняется от них, необязательно посещать медицинское учреждение. Вполне можно воспользоваться глюкометром в домашних условиях.
Особенно это удобно, когда речь идет о совсем маленьких детях. Однако если данные портативного бытового глюкометра показывают, что уровень глюкозы в крови и норма у детей этой возрастной группы не совпадают, есть смысл сдать кровь на анализ в лабораторию, в медицинском учреждении.
Процедура стационарной сдачи крови достаточна проста, и обычно не пугает ребенка. Первично этот анализ берут из пальца.
Если же данные об уровне сахаров после расшифровки окажутся за пределами нормальных для возрастной группы показателей, то берется повторный, более серьезный анализ венозной крови с расшифровкой по таким параметрам, как:
- Исследование соотношения гликированного гемоглобина;
- Толерантность соотношений к уровню сахаров (тест с дополнительной нагрузкой глюкозой);
- Общая картина показателей в крови.
Для того чтобы данные были объективны, необходимо соблюсти ряд предварительных подготовительных ограничений:
- Накануне сдачи крови, нужно исключить прием любых лекарств, и сделать это как минимум за сутки до анализа;
- Перед забором крови, с утра нельзя чистить зубы или жевать жевательную резинку – и то, и то содержит глюкозу, через слизистую рта моментально попадающую в кровь;
- Последний раз кушать можно за 12-15 часов до процедуры, чтобы результаты не были искажены;
- Пить только простую воду, перейти на нее не позднее чем за сутки до анализа;
- Обеспечить ребенку полный покой и отсутствие физических и эмоциональных нагрузок, которые приводят к выбросу гормонов и, соответственно, скачку показателей сахара.
Подробнее о том, обязательно ли сдавать крови из вены натощак, читайте здесь.
Эти же правила касаются и домашнего анализа глюкометром.
Клиническая картина
Классическая галактоземия – наиболее тяжёлая форма нарушения метаболизма галактозы.
Клинические проявления заболевания возникают в первые дни жизни, отличаются быстрым прогрессированием и при отсутствии лечения приобретают жизнеугрожающий характер.
При вскармливании молоком у ребёнка развивается рвота, послабление стула, мышечная атония, сонливость, вялость. Новорожденный не прибавляет в весе, активность сосания значительно снижается, развиваются проявления поражения печени, в сыворотке крови снижается уровень глюкозы, печень увеличивается в размере, кожные покровы приобретают желтушность; недостаточность свёртывающей системы крови сопровождается кровоточивостью; у многих больных развивается нарушение функции канальцев почек.
Наиболее грозным проявлениям является сепсис, спровоцированный кишечной палочкой, который без соответствующего лечения завершается летальным исходом; кроме того, частым летальным исходом в первые месяцы жизни завершается развившаяся хроническая недостаточность печени.
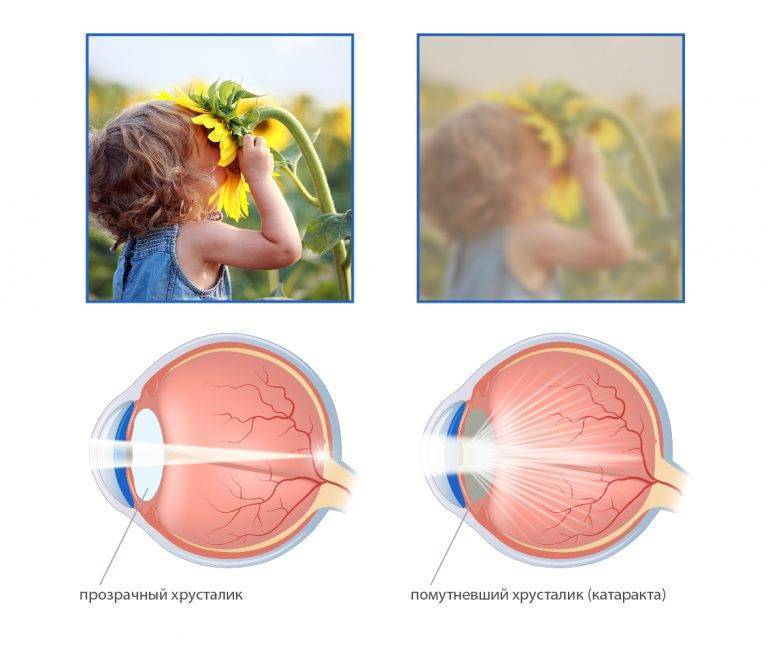
Уже в первые несколько дней после рождения у ребёнка можно выявить катаракту.
У детей, которые выжили, но не получали соответствующего лечения, развивается хроническая печеночная недостаточность, выраженные поражения центральной нервной системы, отличающиеся психомоторным недоразвитием, что сопровождается инвалидизацией и существенным сокращением продолжительности жизни.
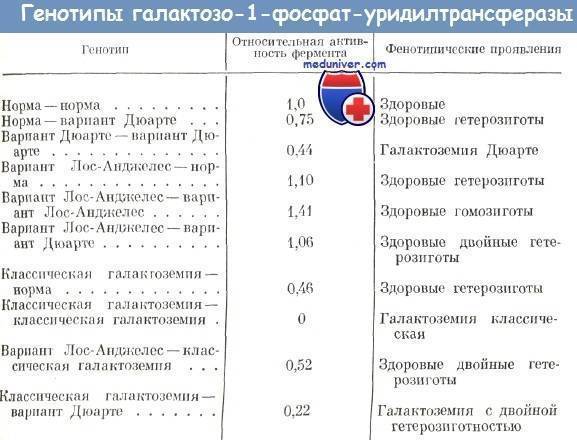
Интенсивность клинических проявлений галактоземии имеет зависимость от величины снижения активности фермента галактозо-1-фосфат-уридилтрансферазы.
При развитии варианта Дуарте активность фермента может колебаться от 5 до 25%. Жизнеугрожающие состояния при таком варианте галактозами развиваются в редких случаях. Однако желтушное окрашивание кожи может сохраняться до двух месяцев после рождения, выявляется увеличенная печень с фиброзными изменениями.
Ребёнок плохо набирает в весе, отмечается отставание физического развития, темповая задержка двигательного развития.
При активности галактозо-1-фосфат-уридилтрансферазы более 50% от нормальной клинические проявления галактоземии не развиваются и носят несущественный характер, специальное лечение не требуется.
Галактоземия 2-го типа встречается значительно реже, частота её встречаемости не выяснена.
Единственным проявлением недостатка галактокиназы у многих больных является развитие катаракты.
Незначительные проявления галактоземии могут развиваться у детей, в рационе питания которых присутствует значительное количество молока.
Зарегистрированы лишь единичные случаи отставания психомоторного развития у детей с галактоземией 2-го типа.
Галактоземия 3-го типа встречается исключительно редко.
Заболевание отличается доброкачественным течением и выявляется случайно при выявлении повышенного уровня галактозы в крови. Катамнестическое исследование позволяет установить взаимосвязь нарушения двигательной функции и развития речи у ребёнка с галактоземией 3-го типа.
Тяжёлая форма заболевания характеризуется сходством клинических проявлений, как и при классической галактоземии включая желтуху, рвоту, мышечную гипотонию, отставание в развитии, увеличение печени и селезёнки, умеренную гипераминоацидурию и выраженную галактозурию.
Даже при ранней диагностике заболевания и своевременно начатом лечении спустя 2–3 года нередко выявляется отставание психомоторного развития и нейросенсорная глухота.
При этой форме заболевания снижение активности фермента выявляется в крови, печени и фибробластах кожи, сохраняется высокий риск формирования катаракты из-за нарушенного обмена галактозы.
Лечение
Чем ранее проведены диагностические мероприятия и выявлена патология, тем успешнее лечение галактоземии. Терапия зависит от тяжести состояния. Обычно она длительная и требует слаженной работы врачей и родителей.
Питание
В основе эффективного лечения лежит принцип замены молока миндальными либо соевыми смесями (это безлактозные смеси). Сегодня практически нет проблем с возможностью приобретения смесей и продуктов питания без лактозы. Ассортимент детского питания в супермаркетах и специализированных магазинах огромен. Производители указывают на упаковке состав продукции и предупреждающие надписи (содержит или не содержит смесь молочный сахар).
Прикорм рекомендуется вводить в более раннем возрасте – около 4 месяцев (для здоровых детей рекомендуемый возраст введения прикорма – это около полугода жизни ребенка).
Приблизительно с 4-месячного возраста специалисты рекомендуют начинать кормить ребенка соком. Для этого постепенно и в очень небольших количествах вводятся фруктовые и ягодные натуральные соки. Не стоит вводить сразу несколько видов фруктов! С 4,5 месяцев малыш может попробовать пюре из фруктов, в 5 месяцев – пюре из овощей, а с 5,5 месяцев – первую кашу. Каши готовятся из кукурузы, гречки, риса. Вместо молока используется овощной отвар, альтернатива отвару – каши, разведенные безлактозным молочком. В полгодика ребенку можно давать мясо: выбираются обезжиренные сорта (птица, говядина, кролик), рыбу вводят в 8 месяцев.
Постепенно следует расширять палитру вкусовых ощущений для малыша
Каждый новый продукт нужно вводить осторожно, тщательно следя за реакцией организма на новую еду. Обычно строгое ограничение лактозы соблюдается до 5 лет (после можно частично компенсировать неправильный ферментный синтез, но не всегда!)
Если степень патологии средняя или тяжелая, то диета сохраняется навсегда. Рацион не должен содержать лактозу, сахарозу, крахмал, т.е. то, что обостряет состояние. Углеводы поступают из альтернативных источников (фруктоза).
Применение лекарств
Диагностика галактоземии
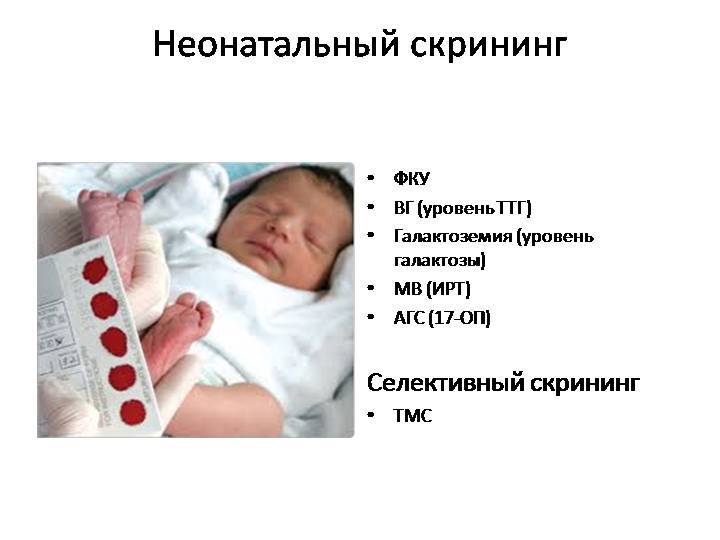
В РФ неонатальный скрининг на ГЕ осуществляют доношенным новорожденным на 4-е сутки жизни, а недоношенным на 7-е сутки жизни. Определяют уровень тотальной галактозы, который в норме < 7,2 мг/дл. Если ее уровень превышает референсное значение, проводят ДНК-диагностику для детекции мутаций в гене GALT. Определяют активность фермента ГАЛТ: снижение его активности в пятнах высушенной крови < 2,5 Е/гHb, в цельной крови < 1,3 Е/гHb является диагностически значимым. Если активность ГАЛТ превышает референсное значение на 50%, а симптомы ГЕ отсутствуют, либо незначительны, специальное лечение не проводится. Успешно проводится и пренатальная диагностика.
Профилактика
Медико-генетическое консультирование: в семье с больным галактоземией ребёнком имеется 25% риск рождения больного ребёнка при каждой последующей беременности. У родственников из группы риска также возможно выявление мутаций, если они были выявлены у больного ребёнка в данной семье.
Пренатальная диагностика с применением кордоцентеза для быстрой диагностики способствует своевременной дифференцировки классической формы галактоземии от форм, связанных с недостаточностью галактокиназы, и другими вариантами, развивающимися относительно благоприятно и без формирования тяжёлых осложнений.
Описание
Галактоземия относится к ряду врожденных наследственных патологий. Встречается это заболевание в медицинской практике достаточно редко.
Связывают развитие патологии с недостаточной активностью необходимых для нормального процесса обмена веществ ферментов, «перерабатывающих» галактозы.
Впервые описали клинику галактоземии в 1908 г. (хотя некоторые относят к данному факту только 1917 г.). К сожалению, но подопытным ребенком стал тот, который страдал истощением, увеличением селезенки и печени. Утверждается, что вся эта симптоматика исчезла после того, как малышу отменили молочное питание.
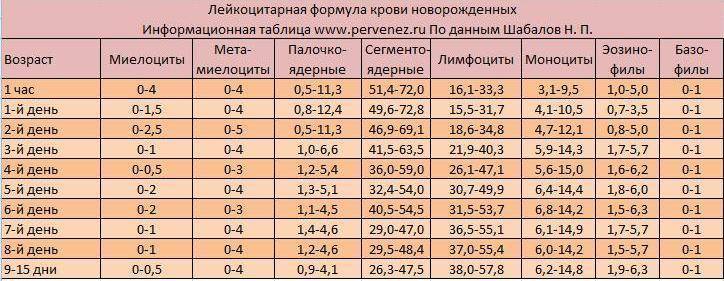
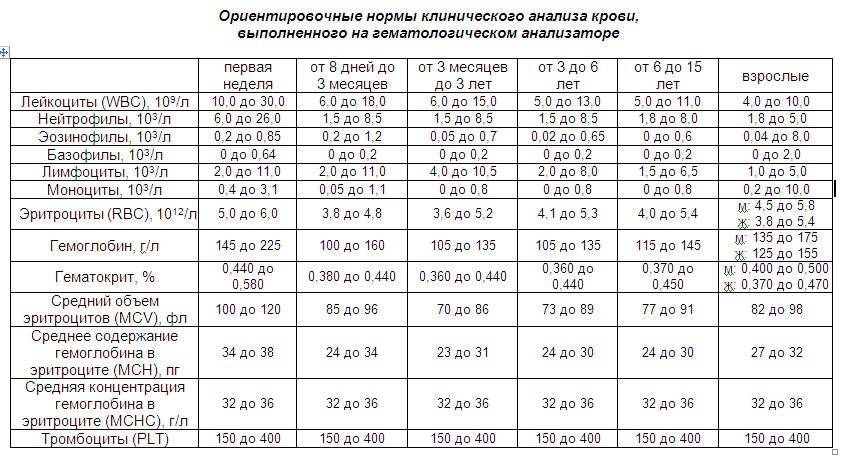
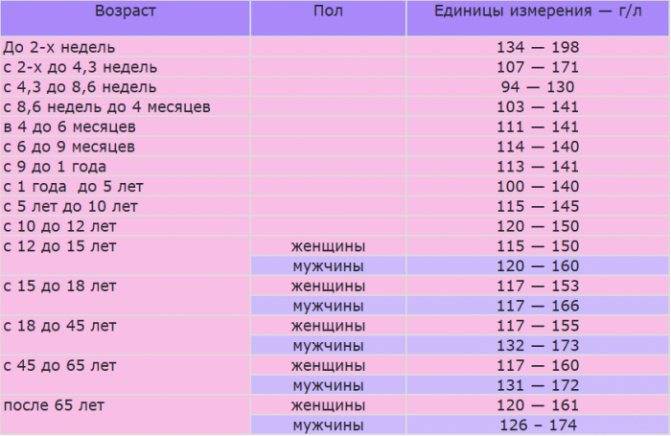
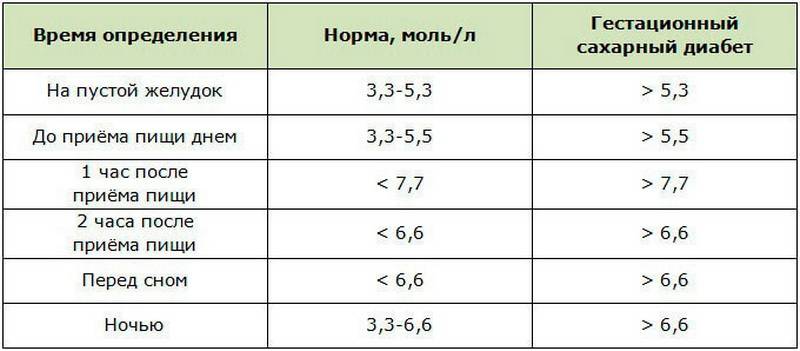
Норма сахара в крови у новорожденных
Чтобы понять, что с анализами новорожденного не все в порядке, для начала нужно выяснить нормы сахара в крови у ребенка натощак и после еды:
| Прием пищи | Низкий уровень (гипогликемия) | Обычный уровень | Высокий уровень (гипергликемия) |
| Натощак (ммоль/л) | Менее 3,3 | 3,3-5,5 | Более 5,5 |
| После кормления (ммоль/л) | Менее 5,3 | До 7,8 | Более 7,8 |
Если сравнивать результаты анализов взрослых и новорожденных детей, они будут существенно отличаться (у последних — в меньшую сторону). Диагноз «транзиторная гипогликемия» не ставят, если показатель уровня глюкозы не опускается ниже отметки 2,2 ммоль/л.
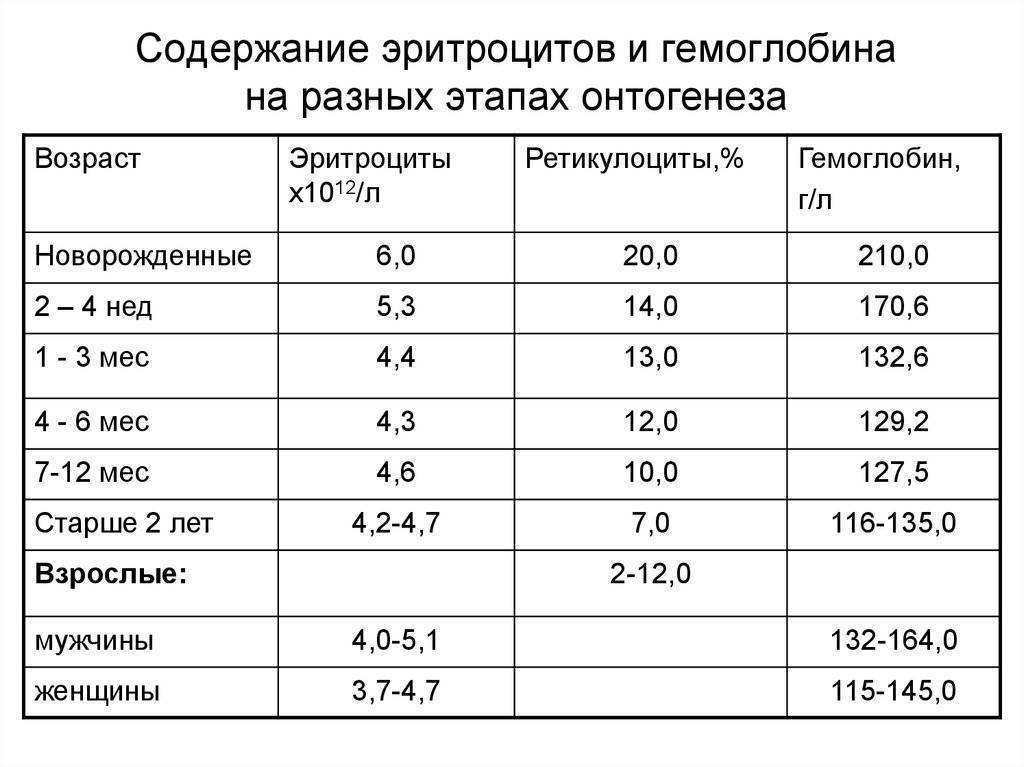
Нормальные показатели уровня глюкозы в крови у детей в зависимости от возраста:
| Возраст | Показатель уровня глюкозы (ммоль/л) |
| Новорожденные | 2,8–4,4 |
| 1 год – 5 лет | 3,3–5,0 |
| Старше 5 лет | 3,3–5,5 |
Диагностика
Для раннего выявления галактоземии медики рекомендуют будущим мамам произвести пренатальное исследование на факт развития этой болезни. С этой целью лучше брать образцы ворсинок и амниотической жидкости.
После рождения малыша ему в обязательном порядке сделают скрининг на галактоземию (совершается забор капиллярной крови) чаще всего скрининг-тестирование проводится несколько раз.
Более редкостным исследованием является анализ мочи ребенка.
В любом случае, результаты анализов будут направлены к педиатру. Только он примет решение о проведении:
- консультации детского невролога и офтальмолога;
- родственной диагностики у родителей ребенка;
- назначении УЗИ внутренних органов (для определения степени их поражения);
- проведении электроэнцефалограммы;
- необходимости назначения биомикроскопии глаз;
- проведении биопсии печени.
Причины
Происходит развитие подобного заболевания только тогда, когда оба родителя являются носителями мутированного гена (то есть по аутосомно-рецессивному типу). Причем каждый из родителей все же будет иметь легкие проблемы в усвоении галактозы.
Как известно, галактоза поступает в человеческий организм вместе с потребляемой пищей, а сама глюкоза должна образовываться в кишечнике в результате гидролизного процесса дисахарида по метаболической системе Лелуара.
А вот при недостаточности (дефиците) важных ферментов (GALK, GALT и GALE) галактоза не преобразуется в глюкозу, а концентрируется в кровяном русле. Как следствие, промежуточные метаболиты галактозы становятся токсичными веществами.
Виды врожденной катаракты
Детские катарактальные хирурги чаще используют классификацию Хватовой А.В.. Врожденная катаракта глаза бывает:
От характера и степени помутнения напрямую зависят сроки хирургического лечения катаракты.
|
Общепринятый возраст малыша, при котором риск минимален – 3-6 месяцев. |
При удалении катаракты в более позднем возрасте, особенно при полных формах, велика вероятность низкого функционального результата из-за развития амблиопии.
Детские офтальмохирурги дополнительно выделяют основные клинические формы врожденных катаракт глаза, такие как:
-
зонулярная. Она отличается наличием оптически прозрачных промежутков в веществе хрусталика. При зонулярной врожденной катаракте острота зрения существенно варьирует от сотых долей до 30-50%;
-
ядерная. Дисковидное помутнение в ядре, от размера которого зависят зрительные функции;
-
полярная. Катаракта захватывает участок передней и/или задней капсулы и прилежащего вещества хрусталика в центре. Помутнения менее 2.5 мм в диаметре несущественно снижают остроту зрения;
-
пленчатая и полурассосавшаяся. Образуются после самопроизвольного лизиса помутнений, характеризуются низким зрением, на уровне 1-4%.
Помимо перечисленных, есть достаточно много других, менее значимых форм врожденной катаракты, практически не снижающих зрение: коралловидная, точечная, порошкообразная и пр.
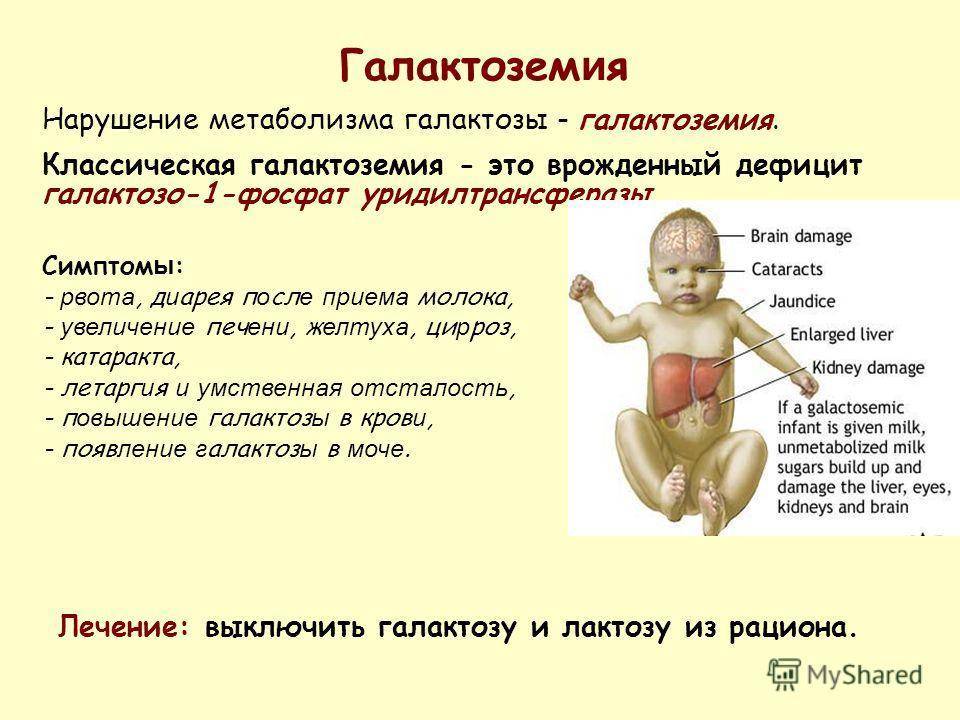
Симптомы
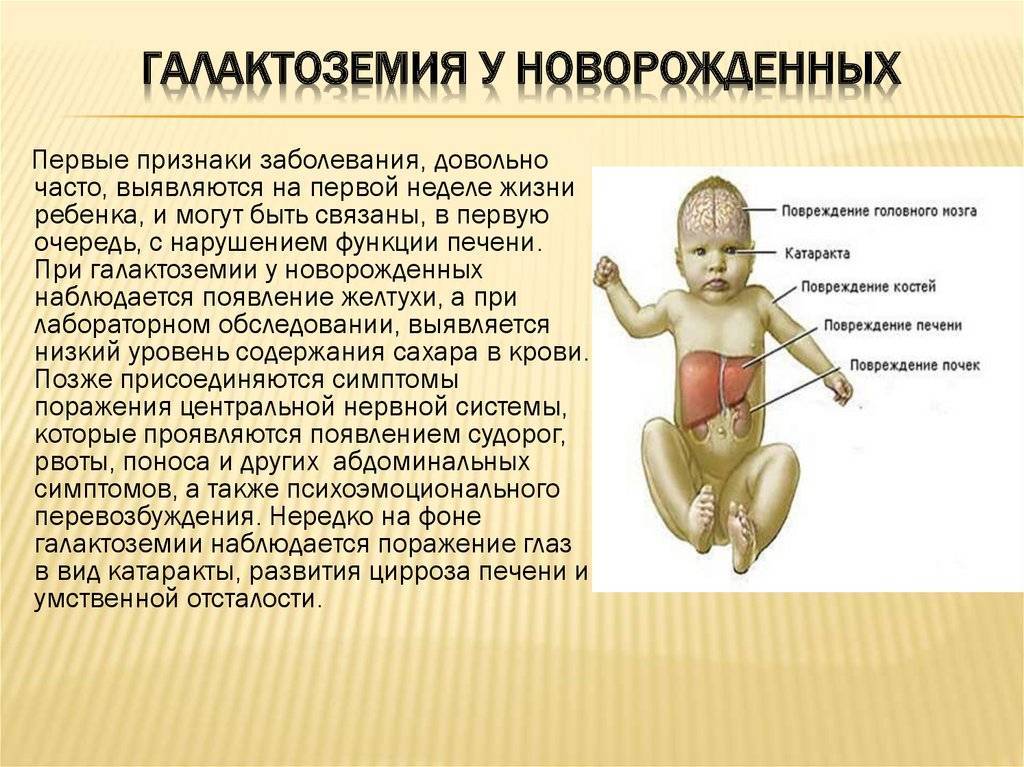
Наиболее важные проявления патологии – это непереносимость любого молока, в составе которого имеется лактоза, а также развитие желтухи, катаракты (сложная болезнь глаз), гепатомегалии, цирроза, истощения ввиду нарушения пищеварения.
Симптомы галоктоземии у новорожденных развиваются из-за значительного повышения концентрации токсичных веществ в крови и появления реакции торможения ферментов на активность токсинов. Ферменты, участвующие в метаболизме углеводов, не могут снизить плотность галактозы (а также ее обменных продуктов), поэтому развивается гипогликемический синдром, оказывающий негативное влияние на ряд внутренних органов.
Распространенные признаки галактоземии. Виды патологии
Классический: обусловлен недостатком галактозо-1-фосфат уридилтрансферазы (это фермент, который участвует в преобразовании галактозы в глюкозу). При недостаточном количестве этого фермента происходит повышение галактозы в крови и уменьшение глюкозы. Печень неполноценно участвует в обмене D-галактозы (составной части молока). Симптомы галактоземии при классическом типе – это большая масса тела новорожденного ребенка. Дополнительно в ближайшее время после родов, после того, как малыш выпьет молоко, у него возникает жидкий стул и/или сильная рвота. Стремительно развивается гипотрофия (дефицит массы тела, истощение), появляется пожелтение склер глаз, кожи. Печень увеличивается, развиваются признаки катаракты (она вызвана образованием галактита в глазном хрусталике по причине расстройства электролитного баланса и повышения галактозы). Часто развивается гемолитическая форма анемии (распад эритроцитов).
Недостаточность галактокиназы проявляется только одним признаком – развитием катаракты. Чтобы понять, что у новорожденного ребенка развивается именно галактоземия, исследуются биологические жидкости. Анализ крови покажет увеличение галактозы и галактитола. Моча насыщается восстанавливающими веществами. Симптомы катаракты развиваются очень быстро, и галактоземия прогрессирует при отсутствии лечения. При своевременной терапии патологические процессы в глазах обратимы.
Недостаточность эпимеразы мало изучена. Патология этого типа почти не имеет физических проявлений, отмечается биохимическими сдвигами, выявляемыми случайно (обнаруживается повышение моносахарида). Данный тип болезни не требует экстренной терапии.
Галактоземия у новорожденных выдает симптоматику в первые 3–10 дней после рождения. В организм ребенка поступает молоко, а вместе с ним вещества, которые не могут перевариться и усвоиться. Постепенно токсины накапливаются. Метаболизм фермента протекает в печени, после чего он поступает в кровяное русло.
Лечение галактоземии
Основным способом терапии ГЕ выступает пожизненная диета с полным исключением галактозы и лактозы: все виды молочных продуктов и продуктов, где оно может содержаться. Широко применяются специальные сухие смеси на основе изолята соевого белка: Нутрилак Соя, Нутрилон Соя, Фрисосой, Хумана СЛ. Если имеется аллергия на белок сои, то назначают смеси на основе гидролизатов казеина: Прегестимил, Нутрамиген, Фрисопеп АС. Их вводят в рацион больного неспешно, на протяжении 5-7 дней и вначале дозы составляют 1/5-1/10 часть от необходимой суточной потребности, параллельно сокращают долю женского молока, либо молочной смеси вплоть до окончательного прекращения. Контроль адекватности лечения осуществляют определяя тотальную галактозу в сыворотке крови 1 раз в 3 месяца, ее считается приемлемым в пределах 5 мг/дл. Если у новорожденного развивается клиническая картина классической ГЕ, то проводят терапию желтухи, сепсиса, патологии почек и ЦНС: борьбу с гипергидратацией, стабилизация уровня глюкозы в крови, антибактериальную терапию, лечение гипокоагуляции. Дети развиваются нормально при наиболее возможных ранних сроках введения диетических ограничений. При поздно диагностированной ГЕ прогноз пессимистический.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Нутрилон Соя (сухая смесь на основе изолята соевого белка). Режим дозирования: назначается внутрь для питания детей с момента рождения до 1 года. 1 мерная ложка вмещает 4,3 г порошка. 100 мл смеси Нутрилон Соя готовятся из расчета 3 мерных ложки на 90 мл воды, что соответствует 66 ккал. Индивидуальная дозировка проводится в соответствии с таблицей кормления.
- Прегестимил (сухая смесь на основе гидролизатов казеина). Режим дозирования: кормление начинают разбавленной в два (34 ккал/100 мл) или более раз смесью в дозе 5–10 мл в сутки. Далее в течение 3–5 дней повышают концентрацию смеси до стандартного разведения, а объем ее увеличивают до значений, соответствующих возрастным особенностям ребенка.