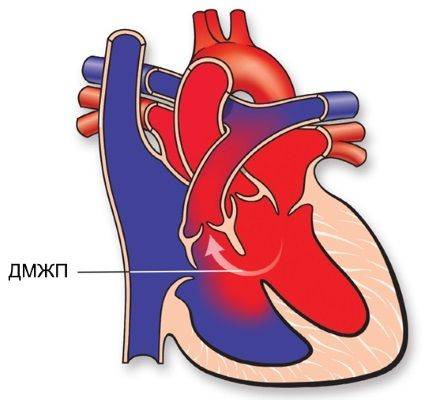
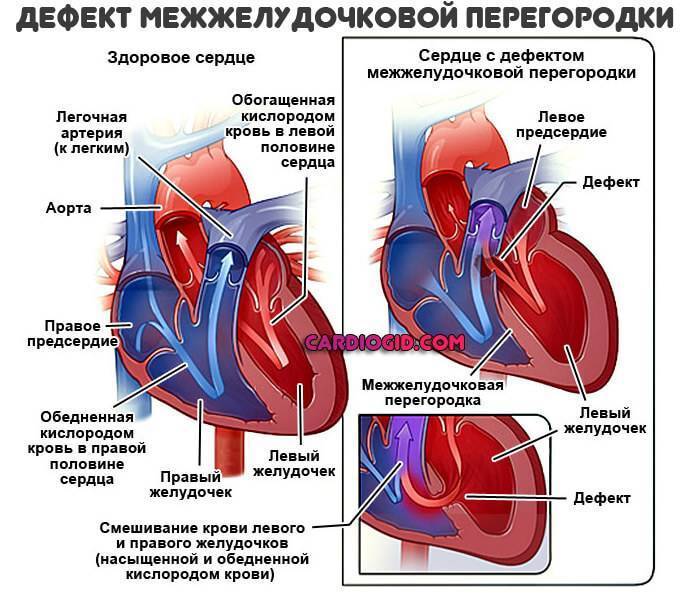
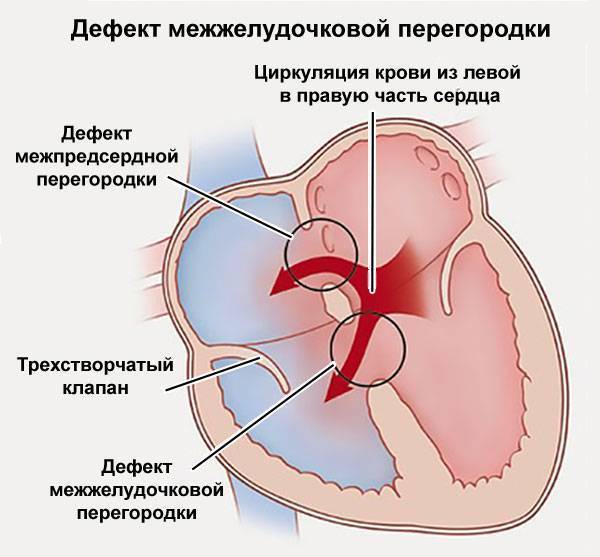
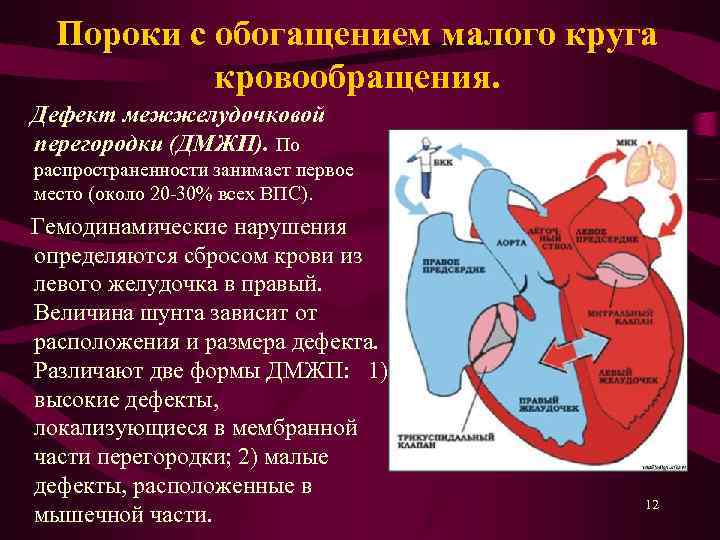
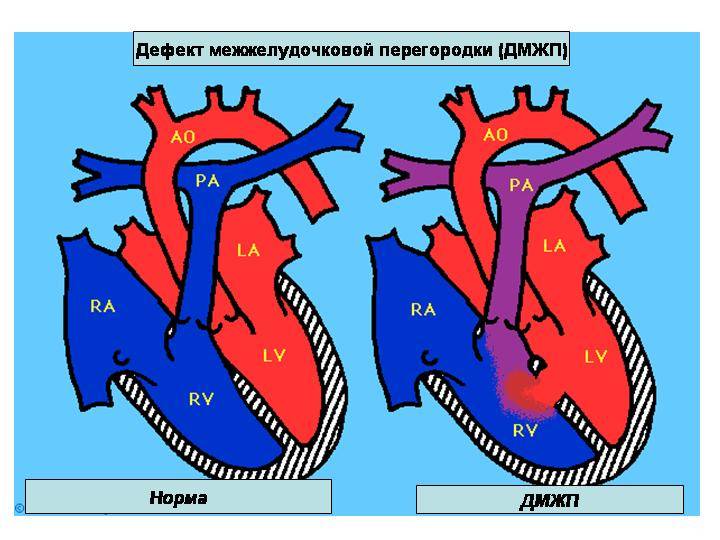
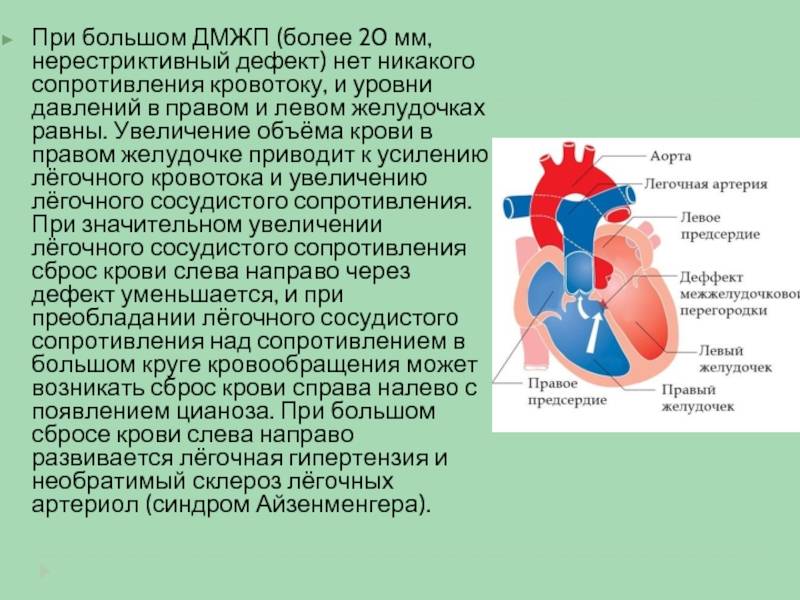
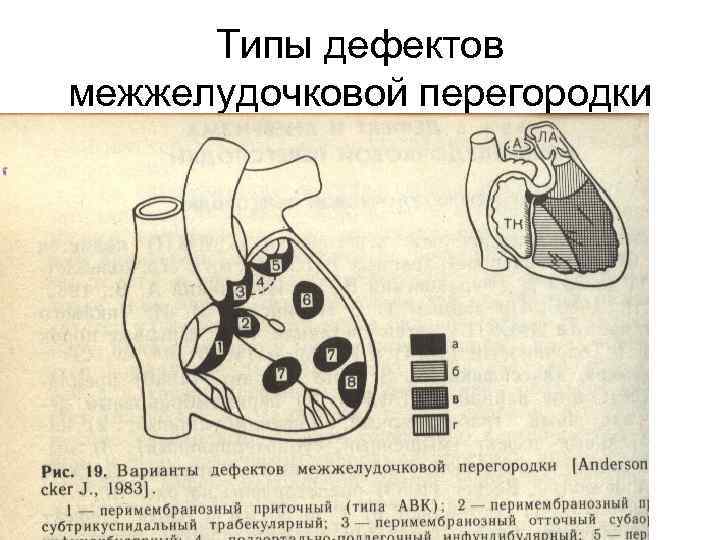
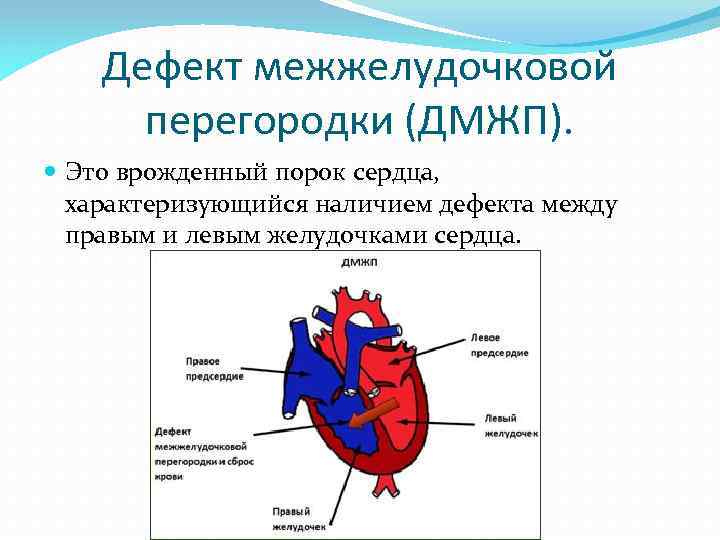
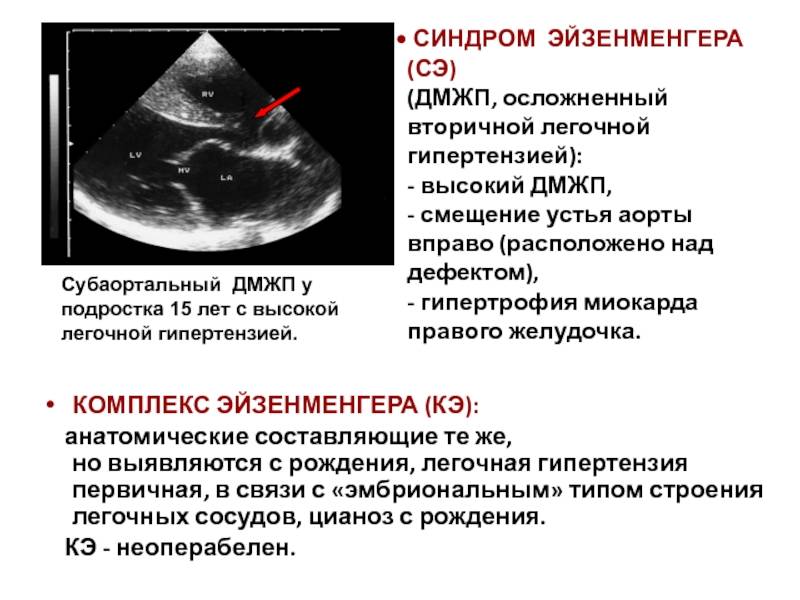
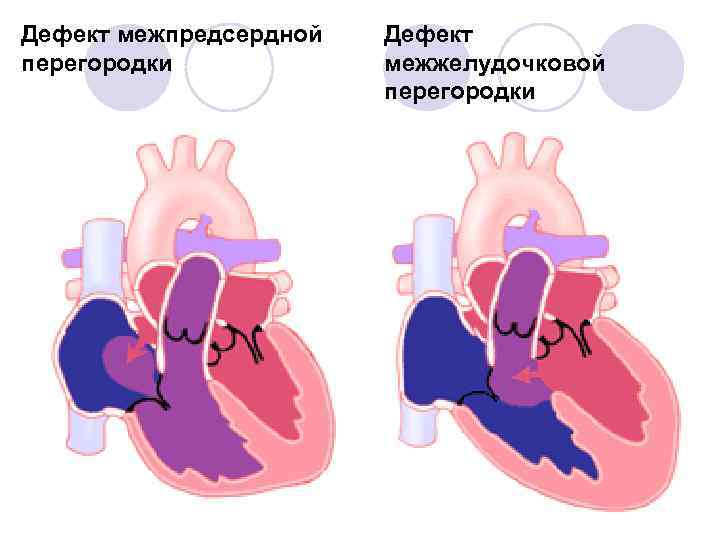
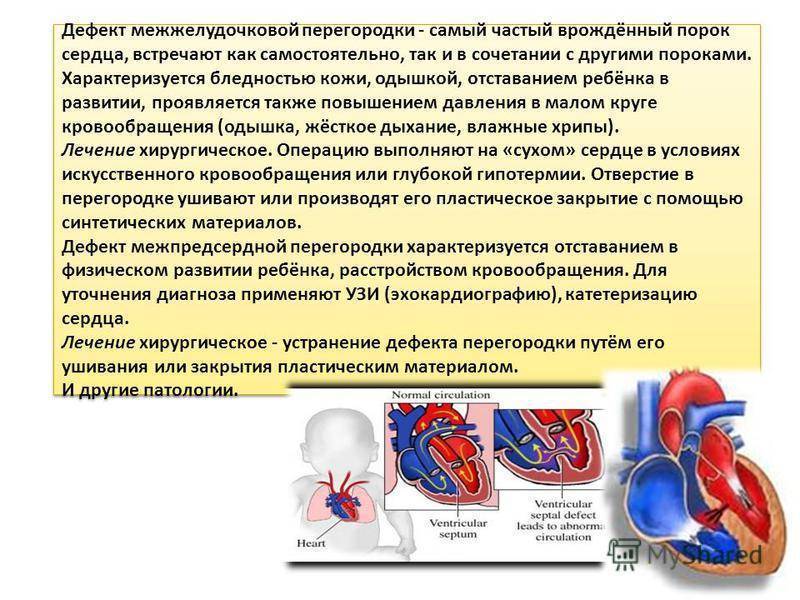
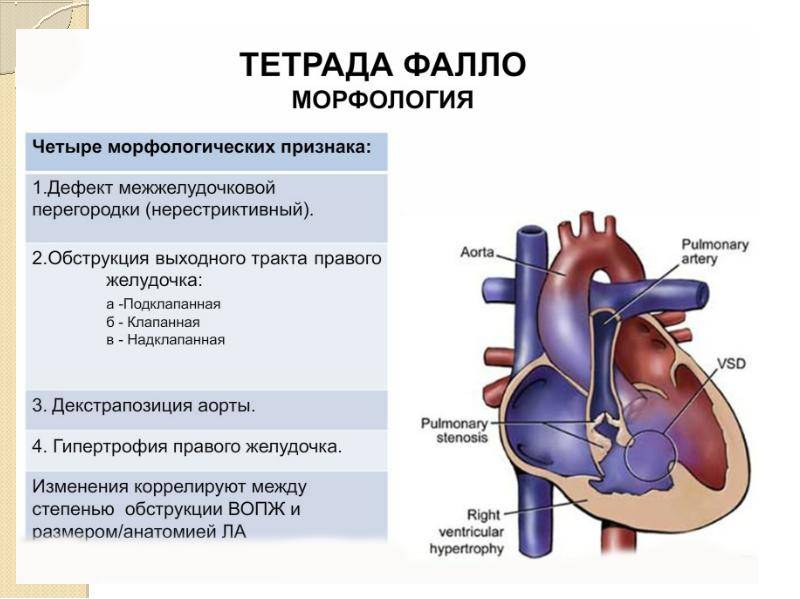
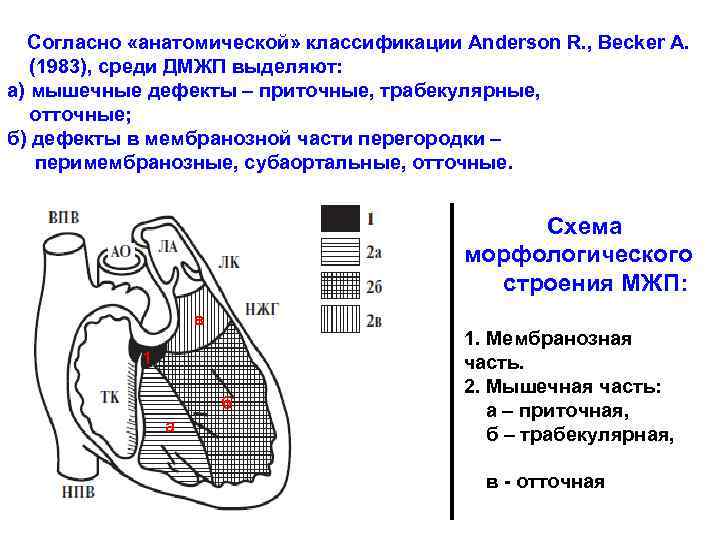
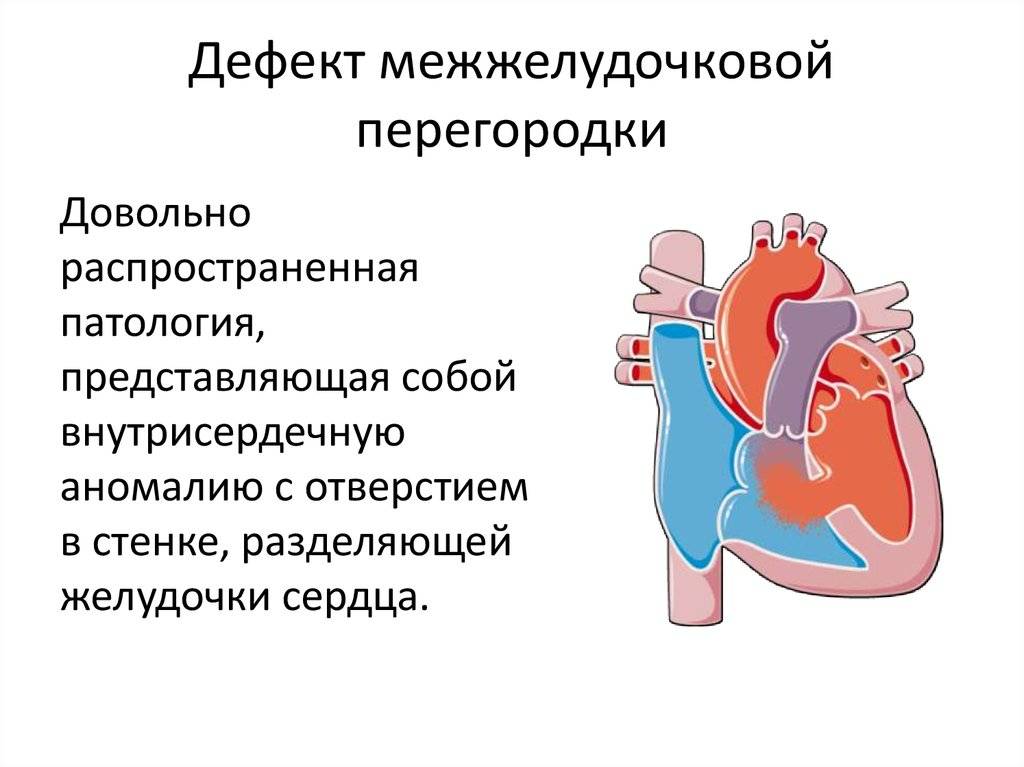
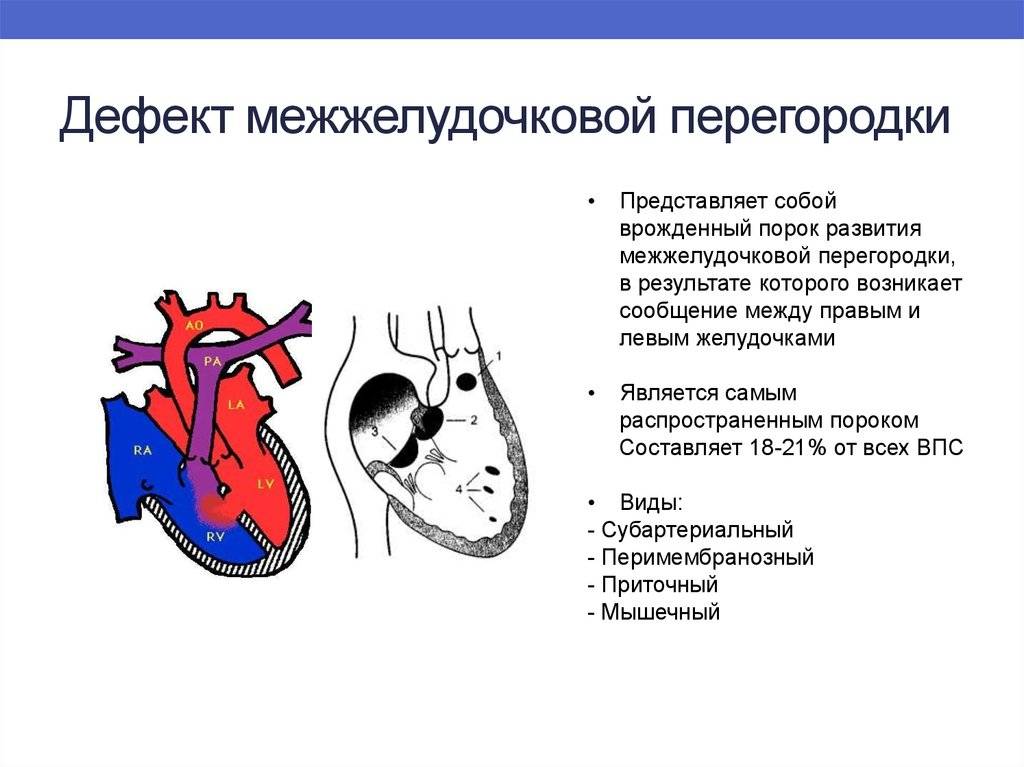
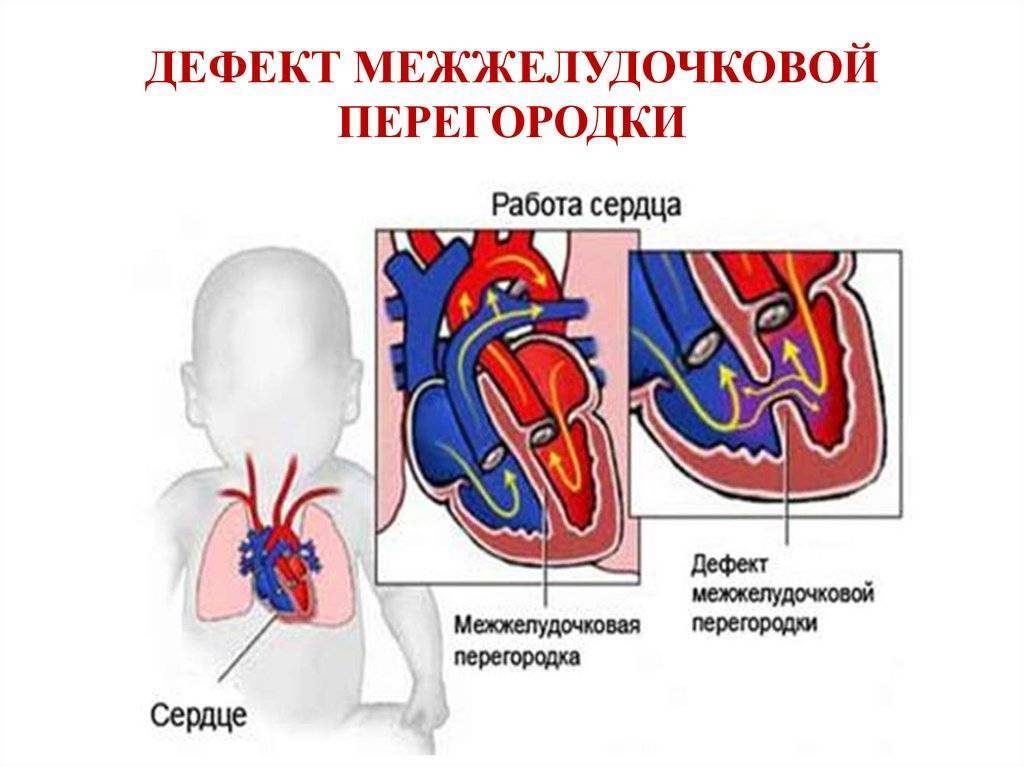
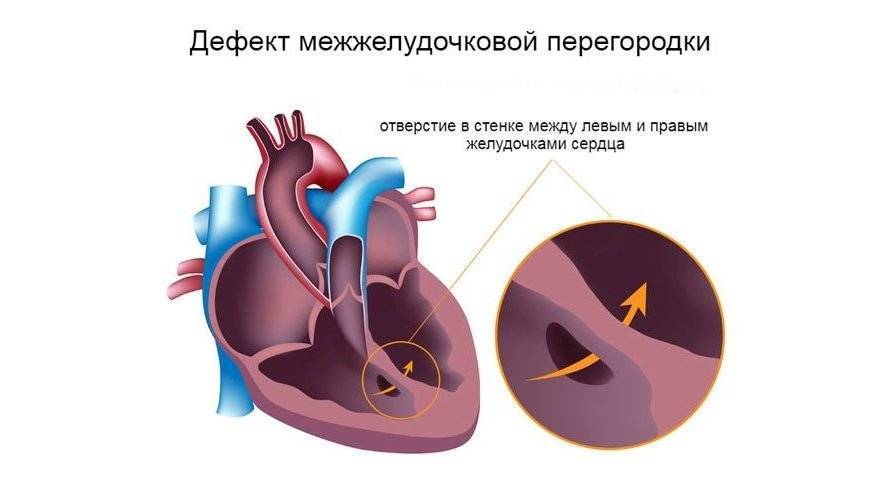
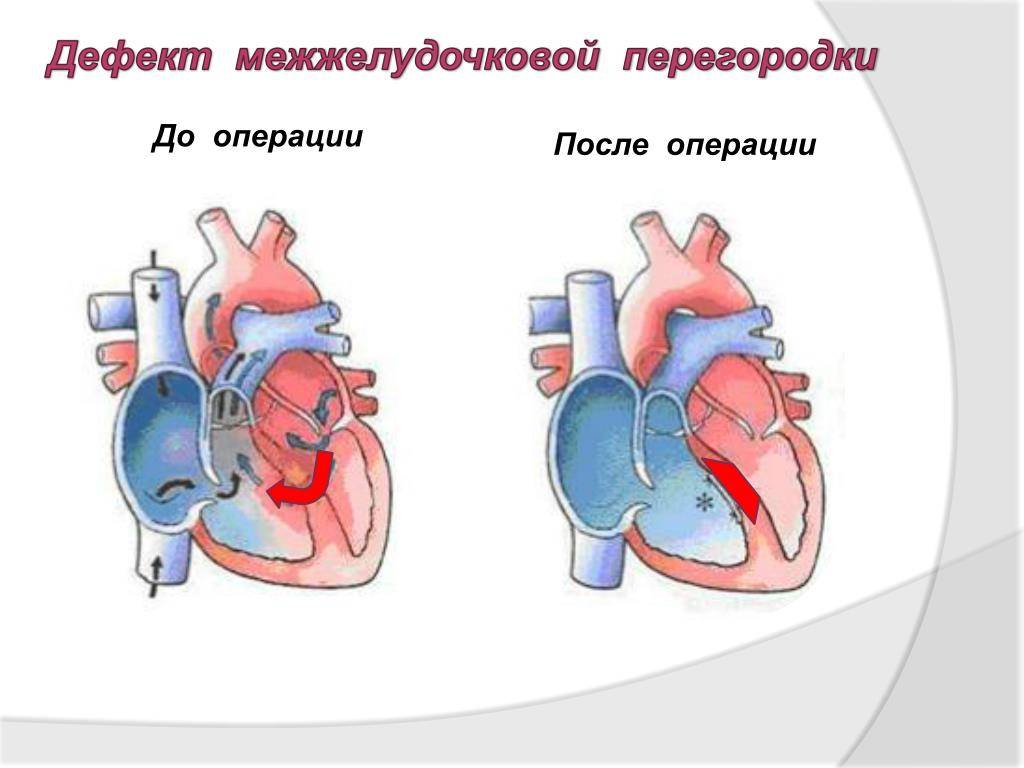
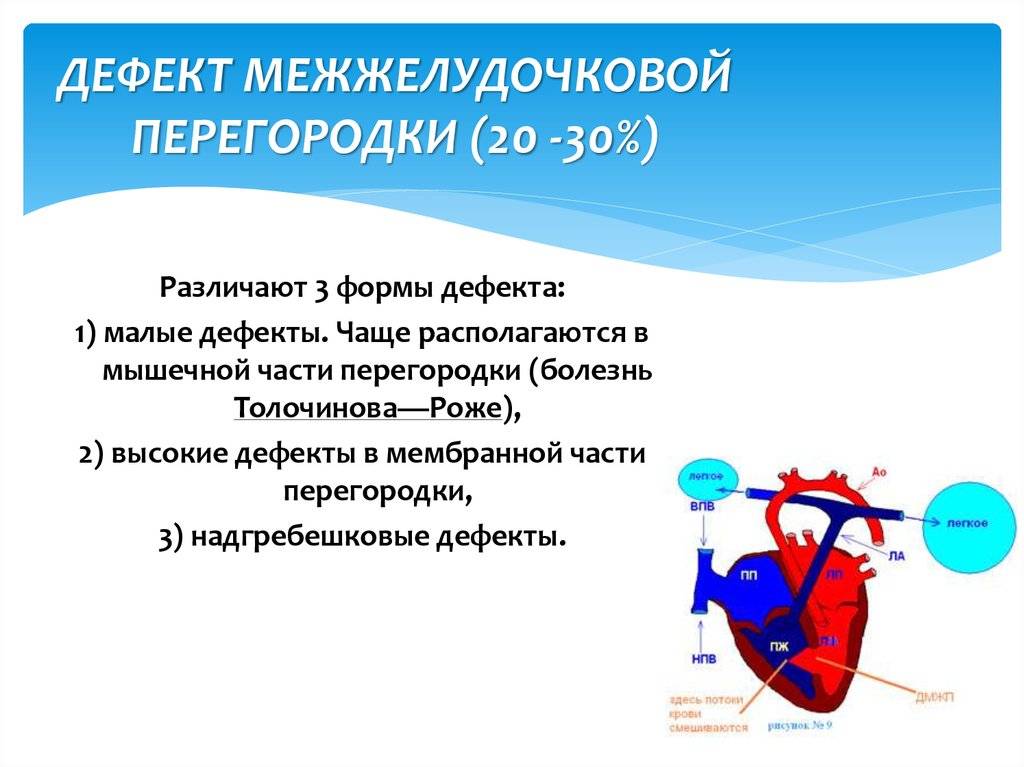
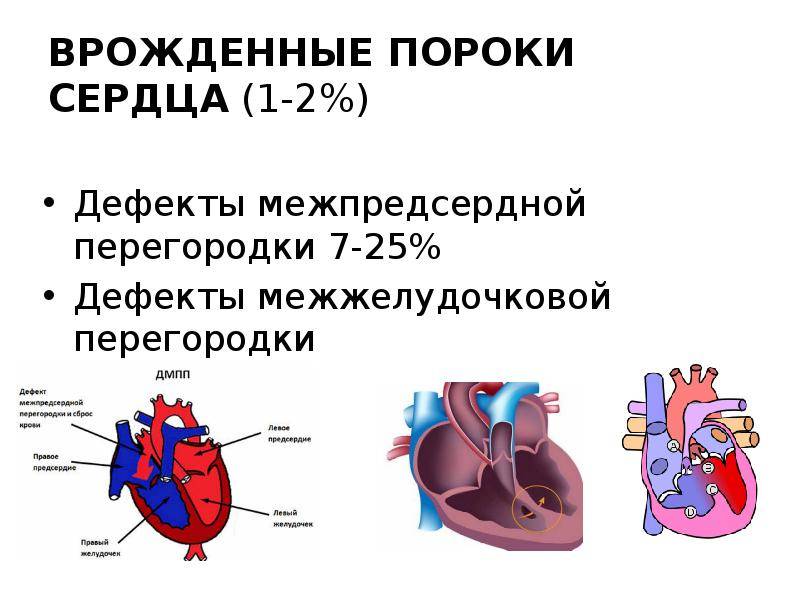
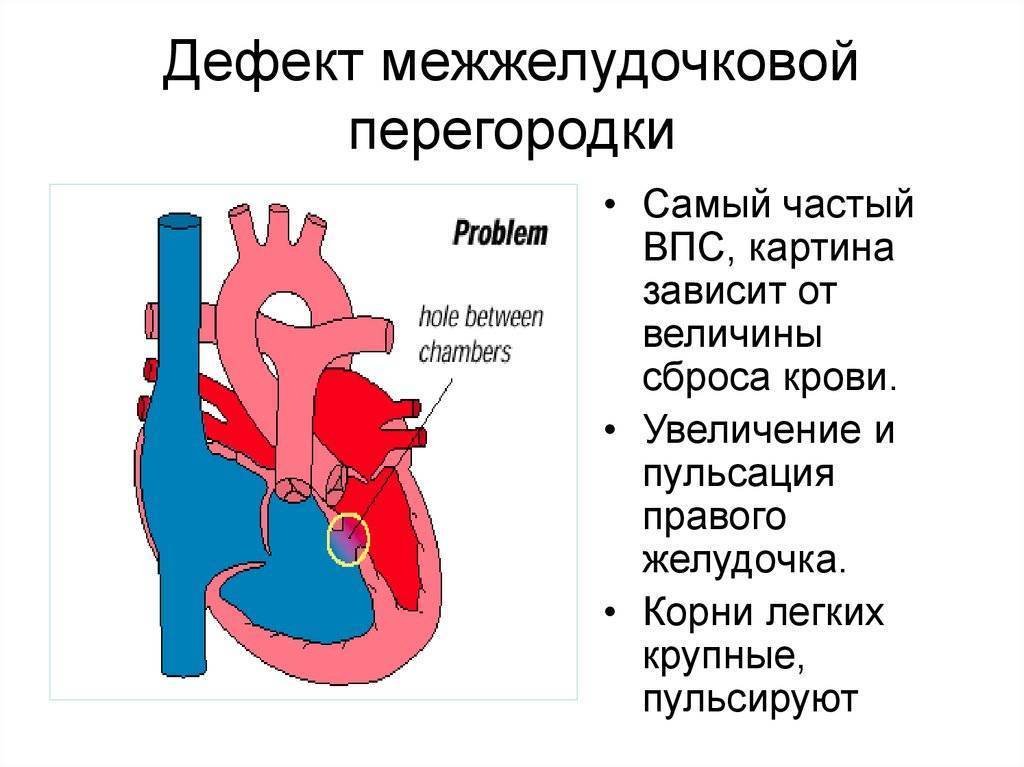
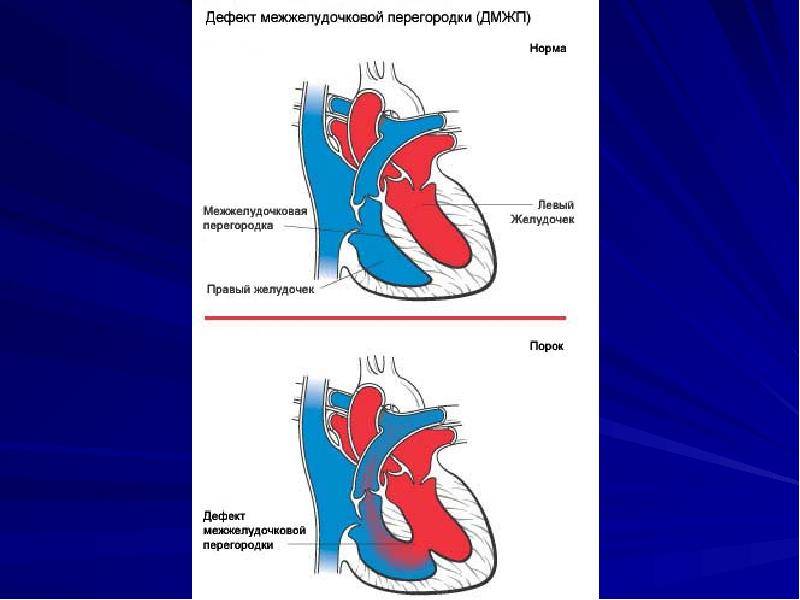
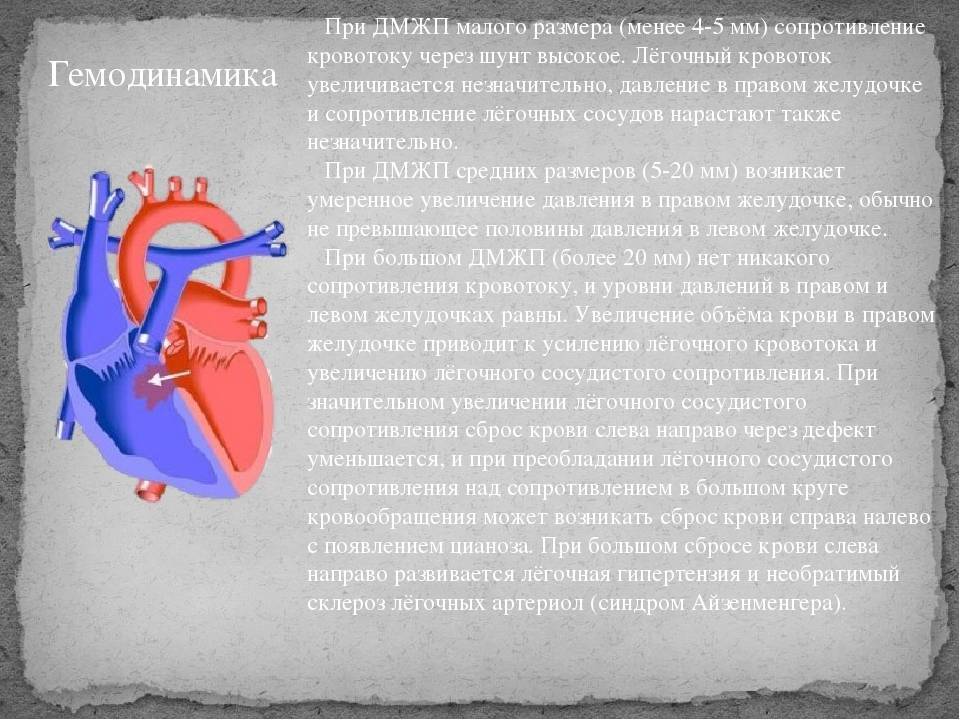
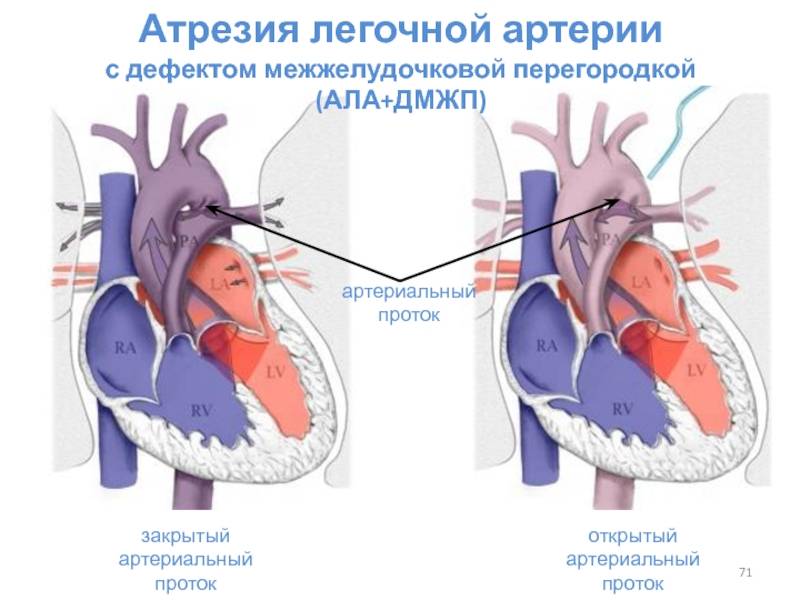
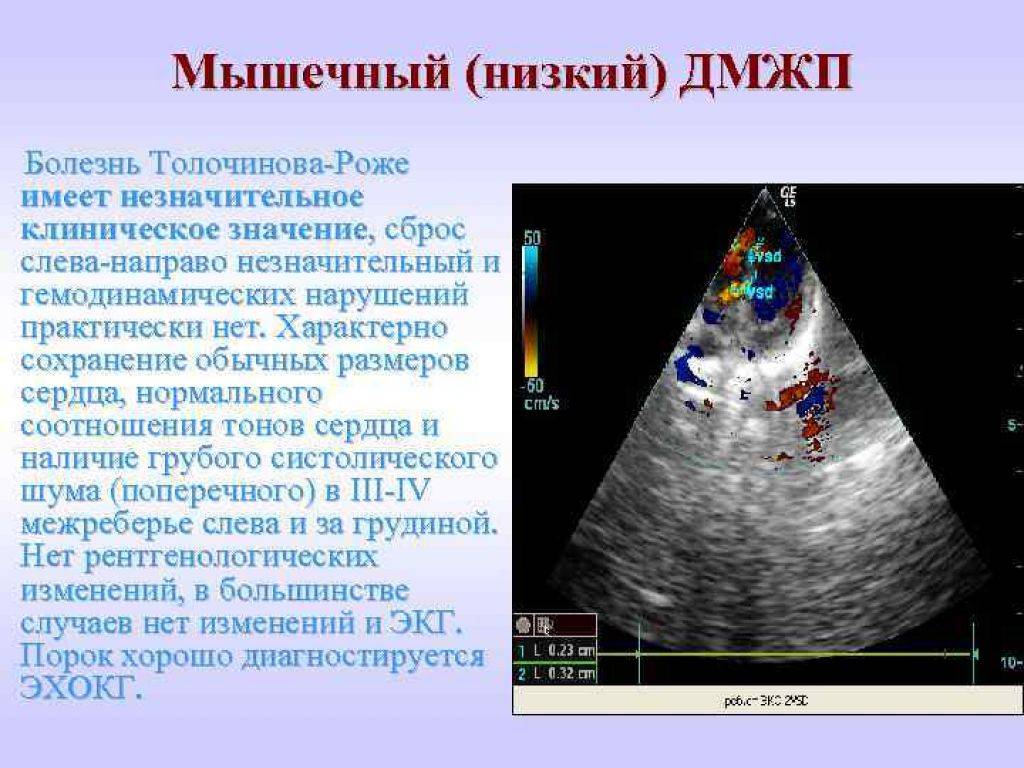
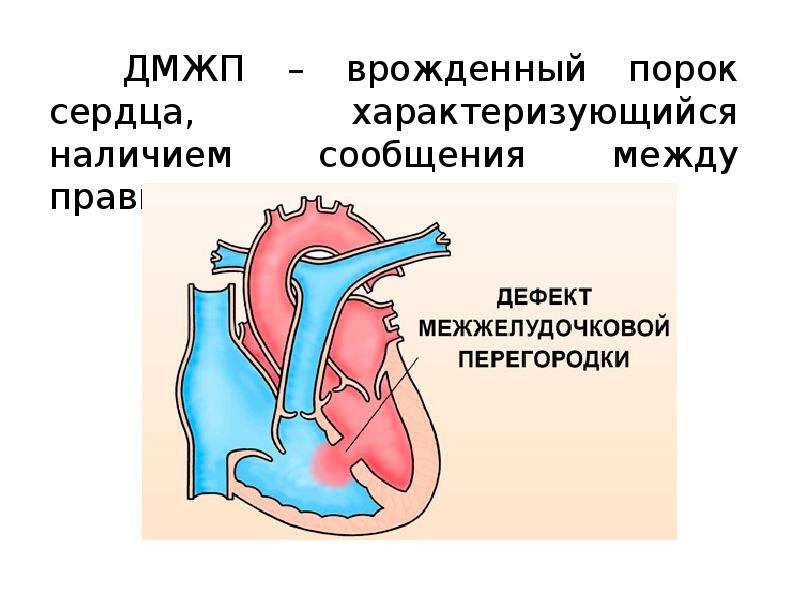
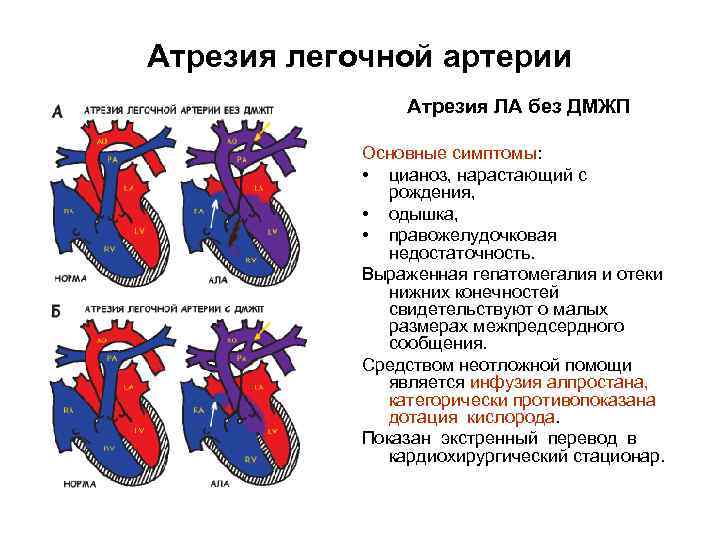
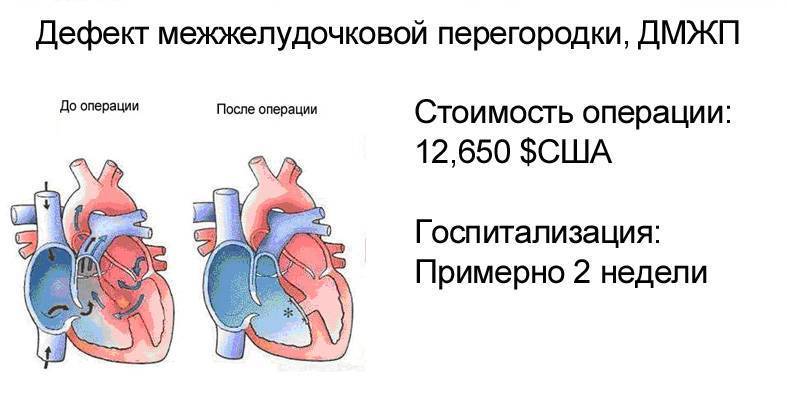
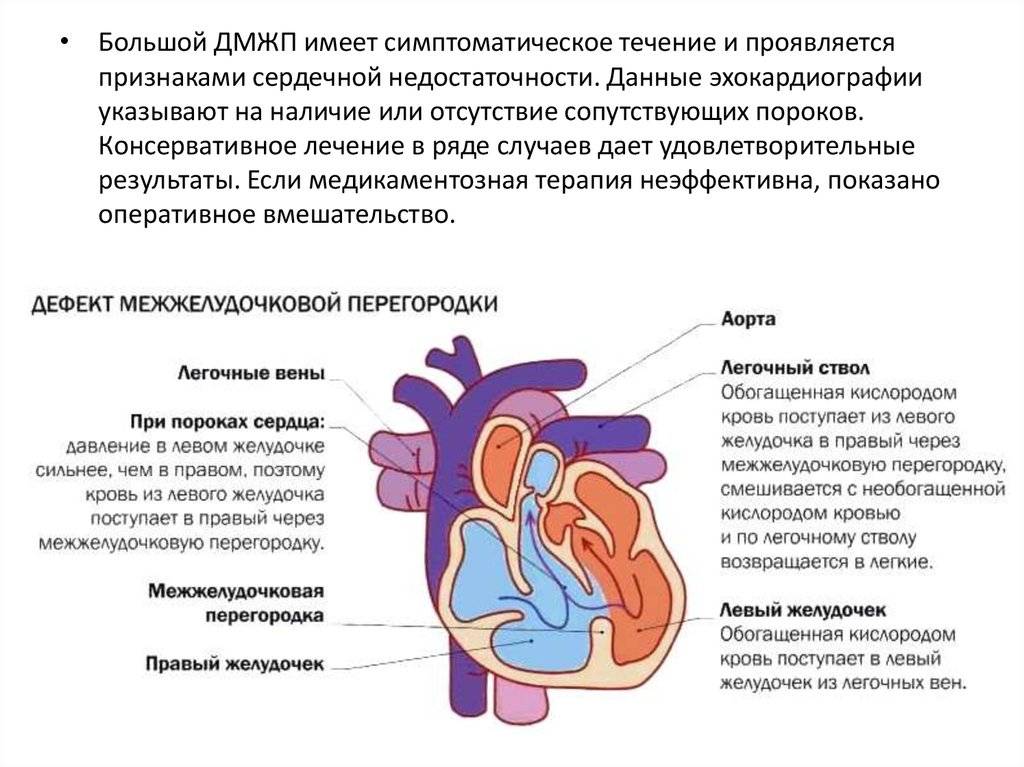
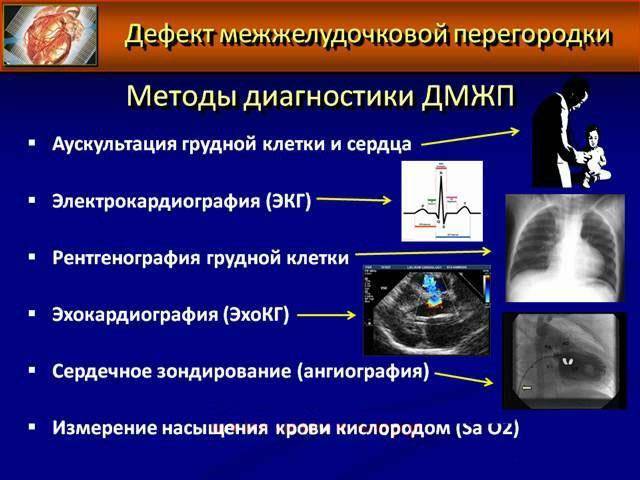
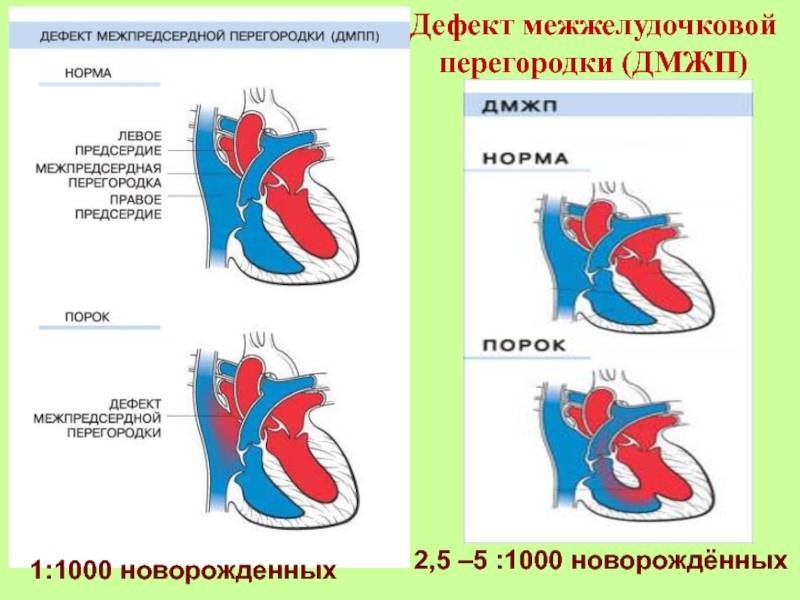
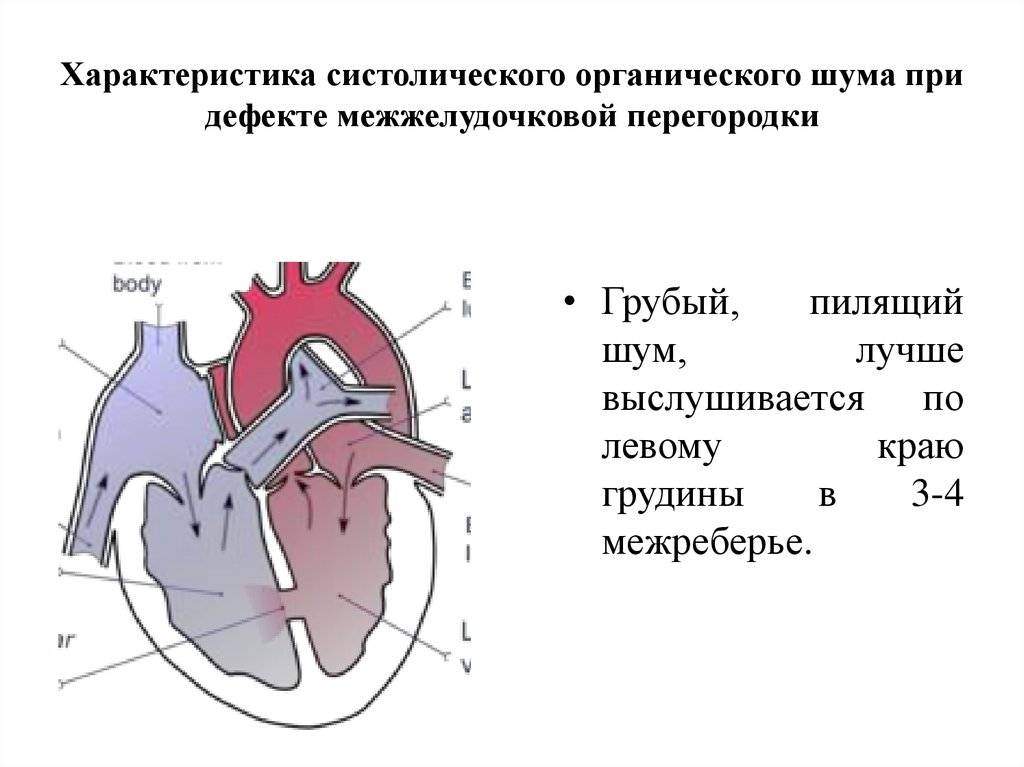
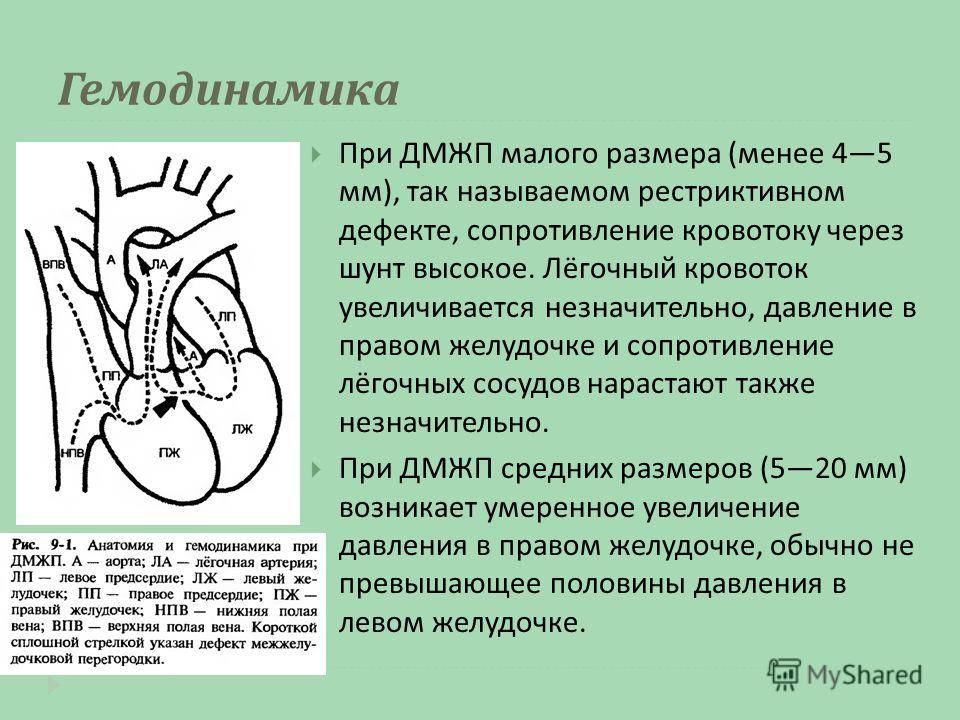
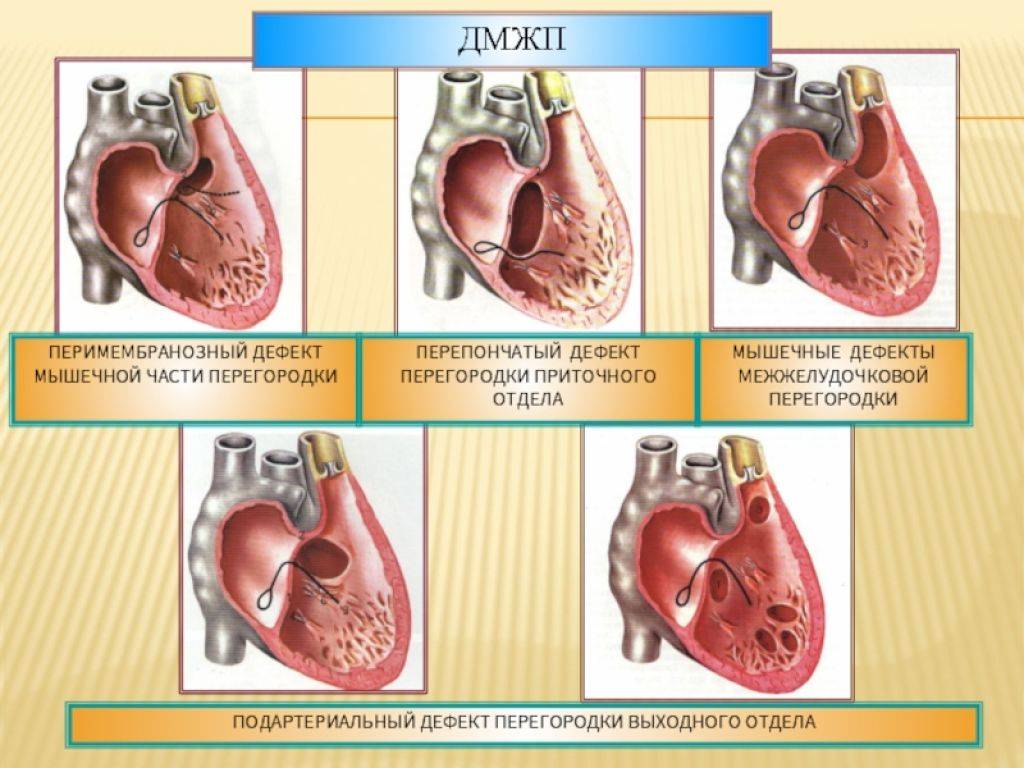
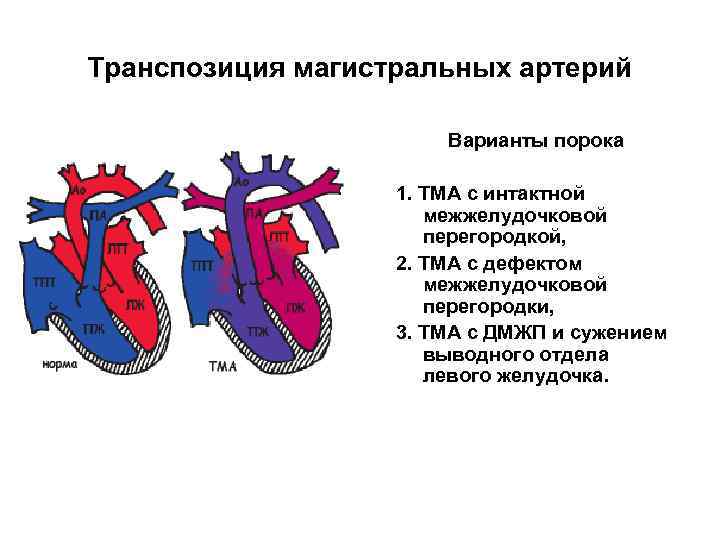
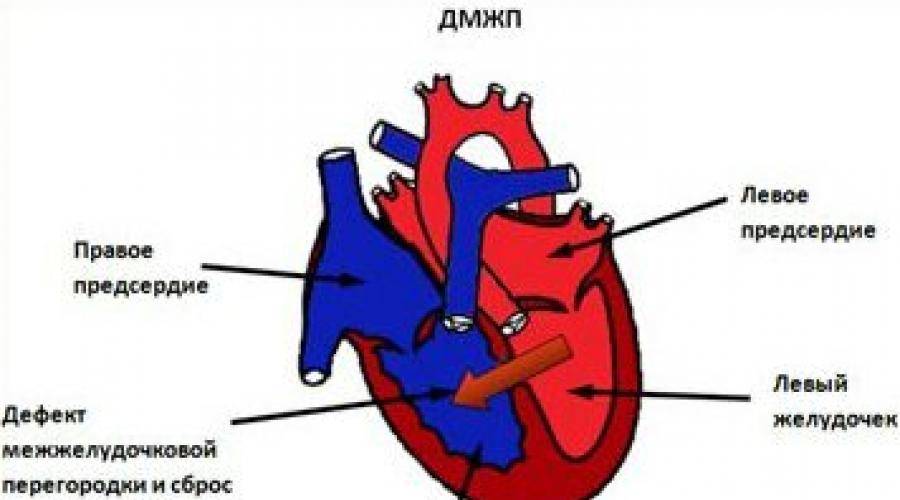
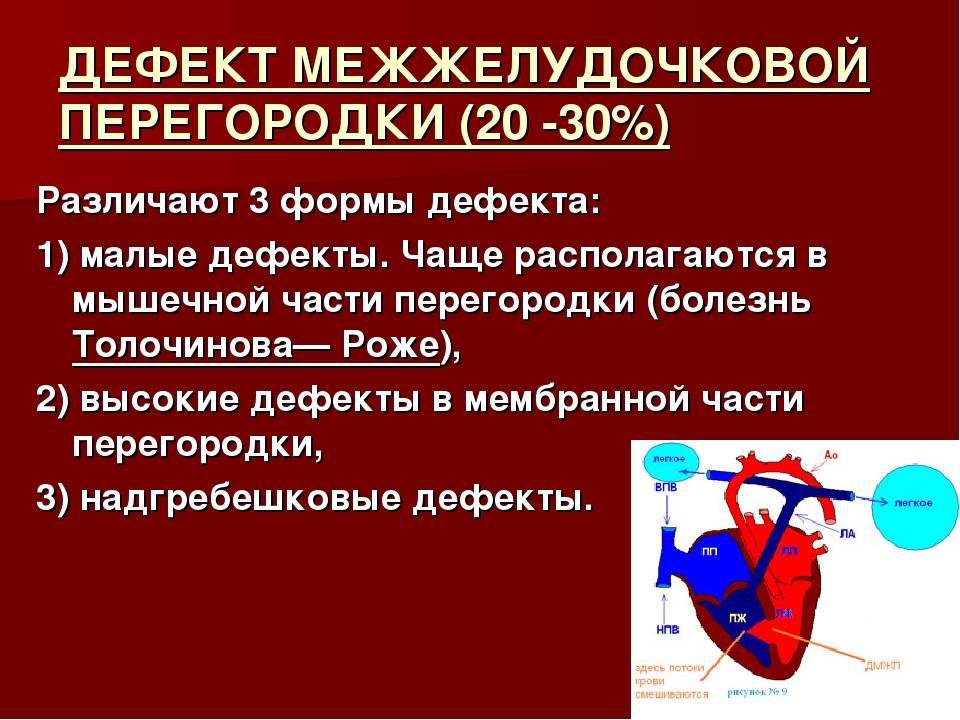
Диагностика при ДМЖП
Диагностические ультразвуковые исследования выявляют ДМЖП еще на этапе внутриутробного развития. С их помощью также подтверждают и уточняют диагноз после рождения ребенка. При необходимости могут дополнительно назначаться инвазивные методы обследования, невозможные во время внутриутробного развития. Помимо осмотра врача проводится:
электрокардиография. Результат может быть как нормальным, так и с признаками перегрузки правых отделов сердца. Иногда при их перерастяжении страдает проводящая система, в итоге развивается аритмия, и это тоже отражается на ЭКГ
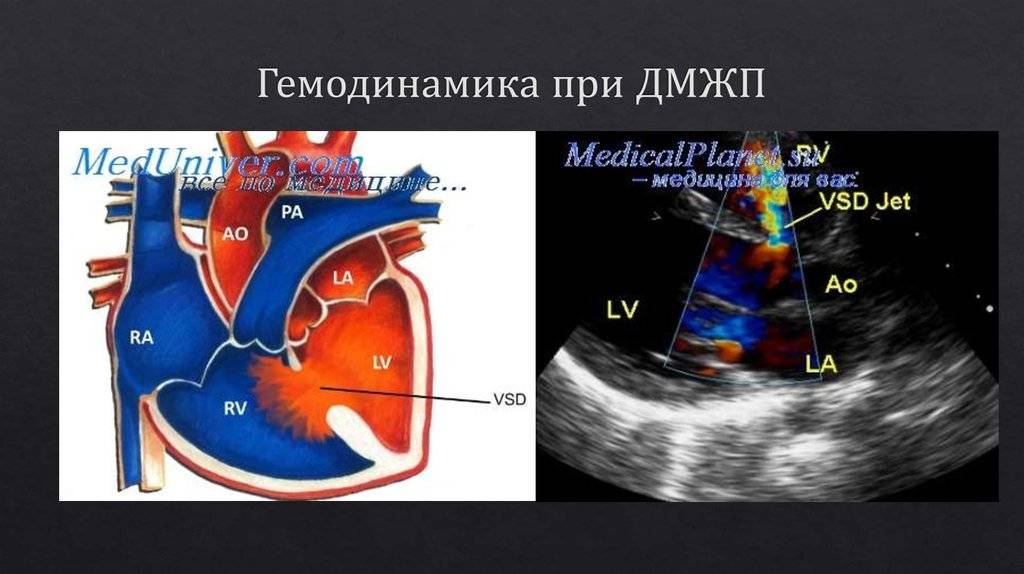
эхокардиография позволяет оценить размеры ДМЖП, особенности кровотока в полостях сердца и состояние всех его отделов
цветное дуплексное сканирование необходимо для уточнения результатов, полученных ранее, определения местоположения дефекта на перегородке
Это важно для выбора техники закрытия дефекта и используемых при этом материалов
зондирование сердца с помощью введенного через периферические сосуды катетера назначается, если после других методов исследования остались неясные вопросы
Необходимость в проведении всех этих методов возникает далеко не всегда. Опытные специалисты часто получают все нужные данные уже после нескольких диагностических тестов.
По результатам обследования может быть принято решение о хирургическом лечении, если:
- ДМЖП слишком велик, имеются и быстро нарастают признаки сердечной недостаточности. Промедление в таких случаях слишком опасно
- по мере наблюдения ребенка ДМЖП не уменьшается
Как правило, хирургическое лечение ДМЖП проводится одномоментно и состоит в ликвидации патологического сообщения между желудочками. Однако иногда ребенок находится в тяжелом состоянии, и радикальная операция для него слишком рискованна. Тогда ему назначают консервативную терапию для борьбы с сердечной недостаточностью и «разгрузки» правых отделов сердца. И на этом фоне в качестве первого этапа хирургического лечения неплотно перевязывают ствол легочной артерии, суживая ее просвет. В течение нескольких месяцев это позволяет преодолевать повышение давления в малом круге кровообращения. Состояние ребенка улучшается, и на втором этапе выполняют радикальную операцию.
Современный подход к хирургическому лечению дефекта межжелудочковой перегородки подразумевает радикальное устранение отверстия между желудочками в ходе традиционной открытой операции с аппаратом искусственного кровообращения, рентгенхирургического малоинвазивного внутрисосудистого вмешательства или гибридной операции, включающей элементы двух первых.
Классификация дефектов
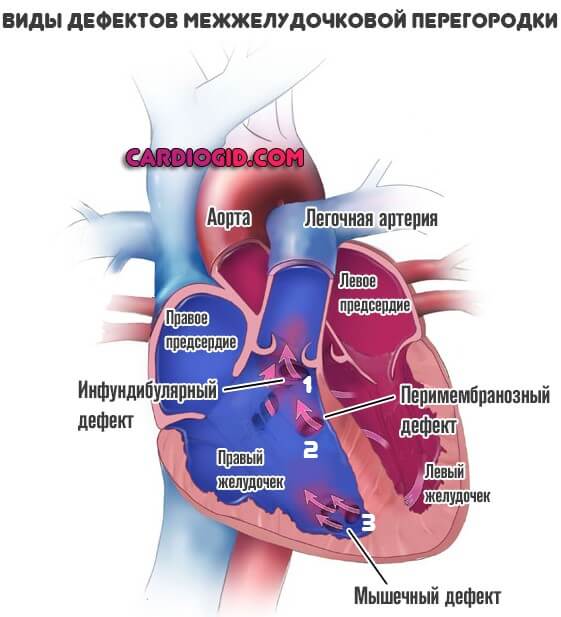
Типизация проводится в зависимости от локализации и тяжести патологического процесса. По первому критерию выделяют три разновидности нарушения:
- Перимембранозный ДМЖП. Встречается наиболее часто. В плане распространенности на него приходится до 85% всех ситуаций. Образуется в верхней части перегородки, под аортальным клапаном.
- Мышечный. Затрагивает мышечную часть межжелудочковой перегородки, удален от клапанов.
- Инфундибулярный. Образуется под клапаном легочной артерии или аорты.
Принципиальной разницы в тактике терапии нет. Единственное, нужно точно знать, где находится нарушение, чтобы проработать щадящий, экономичный доступ.
Размеры дефекта оценивают по отношению к диаметру аортального отверстия:
| Малый | Умеренный | Большой |
|---|---|---|
| Менее 1/3 диаметра (1-3 мм) | 1/2–1/3 диаметра | Равен диаметру или превышает его |
Способ типизации — эхокардиография (ЭХОкг). Степень отклонения выставляется не по размерам окна, а по силе признаков.
Классификации используются специалистами для раннего выявления нарушений, определения характера процесса и выработки эффективной тактики лечения.
Современные виды операций при ДМЖП
Каждая из операций имеет свои показания и предпочтительна в определенных клинических ситуациях. Решение о выборе вмешательства принимается коллегиально с учетом всех обстоятельств. Выполняется:
- Традиционная торакотомическая операция с вскрытием грудной клетки и подключением аппарата искусственного кровообращения. Продолжается около 6 часов и требует довольно длительной реабилитации. Но позволяет одновременно устранить другие аномалии сердца и ликвидировать ДМЖП при любом расположении дефекта. В зависимости от положения и размеров его ушивают или накладывают «заплату» из тканей сердечной сумки (перикарда) пациента или синтетического материала.
- Рентгенхирургическая эндоваскулярная (внутрисосудистая) операция показана в шести случаях из десяти. Может быть выполнена, если ДМЖП – единственный порок сердца у ребенка, дефект расположен не ближе нескольких миллиметров от края перегородки, и вес пациента не менее 5 кг. У совсем маленьких детей настолько узкие сосуды, что не позволяют ввести в них катетер и доставить с его помощью к сердцу окклюдер для закрытия дефекта. Это синтетическое приспособление подбирается в соответствии с размером и расположением дефекта, доставляется в катетере к месту назначения в сложенном виде и там расправляется, перекрывая патологический кровоток. На протяжении полугода, пока окклюдер врастает в окружающие ткани, небольшое просачивание крови сохраняется, но оно не имеет существенного значения. А через шесть месяцев отверстие оказывается уже герметично закрытым, и ребенок становится практически здоровым.
- Гибридная операция проводится кардиохирургом и эндоваскулярным хирургом. Выполняется у маленьких детей с узкими для катетера сосудами, на работающем сердце, без аппарата искусственного кровообращения. Кардиохирург вскрывает грудную клетку, делает прокол в сердце для катетера. Далее эндоваскулярный хирург вводит его и устанавливает окклюдер, как при эндоваскулярной операции.
Симптомы дефекта межжелудочковой перегородки у новорожденных
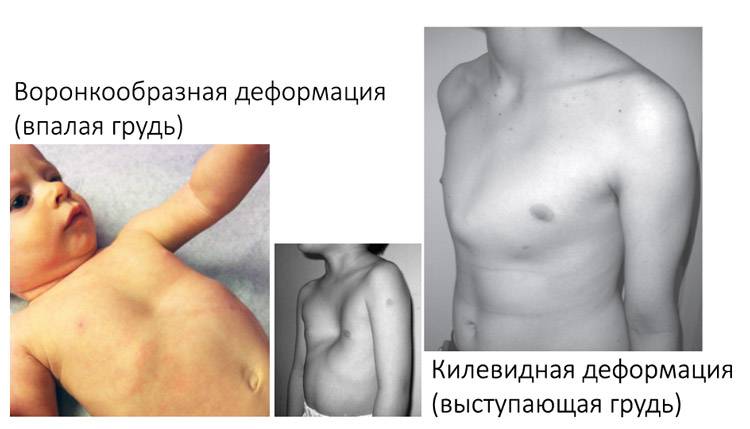
Клиническая картина ДМЖП у новорожденных определяется диаметром сообщающего отверстия. Если он не превышает 10 мм, дети развиваются по возрасту. У них может слегка проявляться повышенная утомляемость, одышка. Со временем наблюдается выпячивающий «сердечный горб» — бугорок в грудной клетке.
Если дефект межжелудочковой перегородки у новорожденных имеет большие размеры, клиника развивается в первые месяцы жизни. Болезнь сопровождается такими признаками:
- синюшность периоральной зоны;
- потливость;
- одышка даже в покое;
- повышенная усталость;
- слабость;
- замедление физического развития, слабый рост;
- тахикардия;
- бледность кожи.
При грудном кормлении такие дети отрываются от бутылочки или груди, захватывают воздух.
Дефект межжелудочковой перегородки у новорожденных приводит к повторяющимся ОРЗ, инфекционным патологиям. В 3-4 годам детей начинают беспокоить боли в сердце, прослушиваются шумы. Границы сердца увеличиваются.
Методы исследования
Заболевание может быть выявлено на плановом обследовании у кардиолога в первый год жизни ребенка. Если этого не произошло и появились явные симптомы, производится сбор анамнеза, пациент осматривается на предмет оценки цвета кожных покровов, характера дыхания, внутригрудных шумов. Далее требуется аппаратная диагностика, которая проводится следующими способами:
- ЭКГ. Показывает перегрузку в работе правосторонней части органа.
- Рентгенография. Проявляет усиленный легочный рисунок, увеличение легочной артерии и сердечной тени на снимках.
- Рентгеноскопия. Фиксирует усиление пульсации легочных корней, что является специфическим симптомом ДМПП.
- ЭхоКГ. Визуально показывает локализацию просвета, определяет его размеры, а также левосторонний сброс кровяной массы.
- Зондирование сердечных полостей. Фиксирует повышение внутрисердечного давления в правосторонних сегментах.
- МРТ сердца. Наиболее информативная методика, способная предоставить полный объем информации о состоянии сердечно-легочной системы, если остальные диагностические методики не показали эффективности.
Лучшим вариантом исследования при врожденных дефектах строения внутренних органов служит МРТ. Без травмирования и болезненности, которые присущи стандартным эндоскопическим и зондирующим методикам, без повышенного радиационного излучения в противовес рентгену, можно сделать полноценное сканирование в любом возрасте, начиная с первых дней жизни. За один короткий сеанс врачи получат исчерпывающие данные об имеющихся нарушениях, что поможет вовремя приступить к лечению, избежать тяжелых последствия в будущем.
Правый желудочек
Функциональная анатомия правого желудочка
Объем правого желудочка у новорожденных составляет 8,5-11 см3,
у детей первого года жизни – 13-20 см3, в 7-9 лет – 28-40 см3,
к 18 годам достигает 150-225 см3. У новорожденных и детей до
1 года длина правого желудочка составляет 4,3-6,2 см, ширина 2,1-3,2
см, у 7-12 летних детей длина желудочка увеличивается до 5-7,2 см,
ширина – до 2-3,5 см. К 18 годам длина правого желудочка достигает
7,3-9,2 см, ширина – 3-5 см. Толщина свободной стенки правого желудочка
у детей до 1 года равна 0,1-0,16 см, к 6 годам она возрастает до 0,2
см, а к 12 годам достигает 0,32 см. Полость правого желудочка имеет
выраженную трабекулярность, при этом основания сосочковых мышц располагаются
в толще трабекул.
Одномерная эхокардиография правого желудочка
Приточный отдел правого желудочка изучают в I стандартной позиции,
отточный в IV позиции. Поперечный размер правого желудочка по данным
эхометрии не соответствует анатомическому поскольку ультразвуковой
луч пересекает полость желудочка в зоне соответствующей 1/3 максимального
поперечного диаметра сферы. Толщина свободной стенки правого желудочка
в одномерном и двухмерном изображении обычно больше, чем анатомическая
из-за выраженной трабекулярности полости. Нормальные значения полости
правого желудочка и толщины его свободной стенки представлены в таблицах
5, 8, 15.
Семиотика правого желудочка
Дилатация правого желудочка
- Идиопатическая дилатация легочной артерии.
- Врожденное отсутствие клапана легочной артерии.
- Частичное отсутствие перикарда.
- Дефект межпредсердной перегородки (первичный, вторичный).
- Аномальный дренаж легочных вен (частичный, тотальный).
- Аномалия Эбштейна (имеется в виду увеличение атриализированной
порции желудочка). - Недостаточность трикуспидального клапана.
- Недостаточность клапана легочной артерии.
- Фистула правой коронарной артерии в правый желудочек.
- Врожденное отсутствие клапана легочной артерии.
- Опухоль правого желудочка.
- Синдром гипоплазии левого желудочка.
- Транспозиция магистральных сосудов.
- Легочная гипертензия (первичная, вторичная).
- Миокардит.
- Застойная сердечная недостаточность.
- Рестриктивная кардиомиопатия.
- Изменение позиции сердца (ротация правого желудочка
кпереди).
Уменьшение полости правого желудочка
- Атрезия трикуспидального клапана.
- Тампонада перикарда.
- Атрезия легочной артерии с интактной межжелудочковой
перегородкой. - Концентрическая гипертрофия правого желудочка.
- Аневризма межжелудочковой перегородки.
- Сдавление правого желудочка объемным образованием
средостения. - Изменение позиции сердца (ротация правого желудочка
кзади).
Гипертрофия свободной стенки правого желудочка
(увеличение толщины стенки более 3 – 5 мм)
- Стеноз легочной артерии (инфундибулярный, клапанный,
надклапанный, стеноз левой или правой ветви легочной артерии). - Легочная гипертензия (первичная, вторичная).
- Рестриктивная кардиомиопатия.
- Опухоль правого желудочка.
- Тетрада Фалло.
- Транспозиция магистральных сосудов.
- У новорожденных, рожденных от матерей,страдающих
диабетом. - Гипертрофическая кардиомиопатия с обструкцией выходного
тракта правого желудочка.
Дополнительные эхосигналы в полости правого желудочка
- Аномальные мышечные пучки.
- Опухоли правого желудочка (чаще рабдомиомы).
- Разрыв аневризмы синуса Вальсальвы в полость правого
желудочка. - Аневризма межжелудочковой перегородки.
- Тромб в правом желудочке.
Двухмерная эхокардиография правого желудочка
Правый желудочек визуализируют во взаимно перпендикулярных осях сканирования:
приточную порцию – в проекции 4-х камер с верхушки и поперечном парастернальном
сечении; отточную – в парастернальной проекции выходного тракта
правого желудочка и поперечном сечении на уровне магистральных сосудов.
Объемная перегрузка правого желудочка
- Дилатация правого желудочка.
- Парадоксальное движение межжелудочковой перегородки
(см) (при наличии легочной гипертензии может не определяться). - Увеличение экскурсии передней створки трикуспидального
клапана. - Систолическое трепетание трикуспидального клапана.
- Уменьшение амплитуды и скорости открытия передней
створки митрального клапана.
Гипертрофия правого желудочка
- Увеличение толщины свободной стенки правого желудочка
более 5 мм. - Гипертрофия (правосторонняя) межжелудочковой перегородки.
- Повышенная трабекулярность полости правого желудочка.
Симптомы пародонтоза
Для пародонтоза характерно длительное течение, так что на ранних стадиях выявить симптомы почти невозможно.
Лазерное лечение эффективно уничтожает инфекцию в пародонтальных карманах, а также регенерирует ткани и снимает воспаление и отеки. В качестве самостоятельной терапии пародонтоза лазер не применяется.
Сначала атрофические процессы, характерные для пародонтоза, постепенно уменьшают размер межзубных перегородок. Затем иногда возникает жжение, боль в деснах, зуд, легкая кровоточивость, неприятный запах изо рта. Десны становятся бледными, шейки зубов оголяются, а сами зубы начинают расшатываться.
Стадии пародонтоза
Более точно симптомы пародонтоза можно описать, распределив их по стадиям заболевания.
- Первая стадия. Практически полное отсутствие симптомов. Изменения в пародонте уже происходят, однако не возникает ни боли, ни зуда десен
- Вторая стадия. Межзубные перегородки уменьшаются, и между зубами начинают регулярно застревать кусочки пищи. Десны иногда кровоточат во время чистки. Появляется легкий зуд, иногда боль
- Третья стадия. Околозубные ткани полностью и необратимо разрушены. Кровоточивость и боль усиливаются, на деснах иногда возникают язвы. Зубы расшатываются окончательно, начинают выпадать
Cтадии пародонтоза
Преимущества эндоваскулярной методики
Эндоваскулярный способ закрытия дефекта выгодно отличается от операции по ушиванию ДМПП. Последняя требует искусственного поддержания кровообращения во время операции, имеет больше противопоказаний и значительный период реабилитации. Несмотря на то, что хирургическое лечение прочно вошло в практику и применялось долгое время, сейчас оно уступает место эндоваскулярному методу.
Главное преимущество в том, что эндоваскулярная операция – это малоинвазивная хирургия. После нее не остается шрамов, процедура не требует разрезов или открытого доступа. У эндоваскулярного метода чрезвычайно низкий процент послеоперационных осложнений. Пациентам не требуется длительная госпитализация и реабилитация.
На данный момент эндоваскулярная операция – это общепризнанный мировой стандарт, отвечающий всем требованиями безопасности и эффективности.
Принцип работы окклюдера
Впервые операция с помощью окклюдера была произведена в конце 80-х годов прошлого века – это был эксперимент на животных. Окклюдер – это специальное устройство, которое устанавливают через сосудистый доступ, а после установки оно выполняет функцию заплатки. Со временем техника выполнения таких операций совершенствовалась, и сейчас успешно применяется для лечения тысяч пациентов. Уже в 21 веке появилось множество модификаций и разновидностей окклюдеров для разных случаев.
Принцип работы устройства следующий: конструкция, раскрывающаяся подобно зонтику, заводится в нужное место через сосуд. После установки заплатки никаких других манипуляций не требуется. Окклюдер производят из сплавов металлов, давно применяемых в медицине – из никеля и титана, покрытых сверху специальным биосовместимым волокном. Материалы протестированы множество раз, они не вызывают аллергии. Устройство сконструировано таким образом, что центровка в отверстии перегородки происходит самостоятельно – задача врача довести окклюдер по сосудам до нужного места. Модель устройства подбирается в зависимости от конкретного дефекта – существуют разные модификации для лечения разных пороков сердца.
Доставка к сердцу производится с помощью катетера, который заводят в крупный сосуд – артерию или вену бедра. Размер окклюдера не больше 2,5 мм в диаметре, поэтому он спокойно проходит по сосудистому руслу. Устройство раскрывается только после установки в соответствующее положение рядом с дефектом перегородки.
Операция выполняется квалифицированными врачами, прошедшими специальное обучение. Процедура проводится в операционной. Пациент во время операции лежит. Врач может контролировать все свои действия с помощью специального оборудования, передающего изображение на мониторы. В ходе операции проводится мониторинг жизненных показателей.
Читать полностью
Врачи, выполняющие эндоваскулярное закрытие дефекта межпредсердной перегородки
Бабунашвили Автандил Михайлович
Врач сердечно-сосудистый хирург, заведующий отделением сердечно-сосудистой хирургии, доктор медицинских наук, профессор, заслуженный врач РФ
Стаж 34 года
Записаться на прием
Причины возникновения ДМЖП у ребенка
ДМЖП у ребенка — врожденная аномалия, которая формируется внутриутробно. Нередко она развивается параллельно с иными пороками — незакрытый артериальный проток, аортальная недостаточность и пр.
Дефект межжелудочковой перегородки у ребенка может развиваться вследствие таких воздействий на организм матери в период вынашивания:
- гормональный дисбаланс;
- инфекции, вирусные заболевания;
- воздействие радиации;
- употребление алкоголя, курение;
- патологии беременности — угроза выкидыша, токсикозы.
Также ДМЖП у ребенка может возникнуть, если будущая мама перенесла инфаркт миокарда.
Чем опасна патология?
На первый взгляд может показаться, что закрытие дефекта межпредсердной перегородки – это не срочная процедура. На самом деле отделы правой стороны сердца несут повышенную нагрузку, со временем они увеличиваются в размерах. Результат – сердечная недостаточность и аритмия, одышка, постоянная усталость, отеки и дискомфорт в области груди. Они могут привести к развитию хронических заболеваний.
От избыточной нагрузки страдает и легочная артерия, с которой начинается малый круг кровообращения. Это приводит к бронхо-легочным болезням. В особо сложных случаях может развиться склероз сосудов легких – необратимое изменение, которое уже не поддается лечению и является противопоказанием для закрытия дефекта
Поэтому важно вовремя начинать диагностику и лечение, не дожидаясь осложнений со стороны сердца и дыхательной системы
У здоровых людей также существует отверстие в перегородке, которое называется овальным окном – и представляет собой небольшую щель между предсердиями. Она формируется еще в период эмбрионального развития и у некоторых остается во взрослой жизни. Если не наблюдается неприятных симптомов, то окно, сохранившееся во взрослом возрасте, не требует лечения и не считается заболеванием. Но в редких случаях оно может вызывать сосудистые патологии – в таком случае предусмотрено хирургическое лечение.
Эндоваскулярное лечение порока сердца – это наиболее современная операция, которая позволяет закрыть дефект перегородки. Если нет осложнений, то рекомендуется проводить операцию в возрасте до 7 лет. Если дефект выявлен позже, то рекомендуется лечение вне зависимости от возраста. При нарастании симптоматики операцию можно проводить даже совсем маленьким детям.
Показания
- наличие дефекта межпредсердной перегородки;
- симптомы перегрузки сердца,
- увеличение отделов сердца.
Противопоказания
- высокая вероятность тромбоэмболии;
- нарушение свертываемости крови;
- индивидуальные реакции непереносимости антикоагулянтов;
- сочетание ДМПП с другими пороками сердца, требующими более сложного вмешательства;
- наличие отверстий в перегородке больше одного;
- диаметр отверстия слишком большой для заплатки-окклюдера;
- острое инфекционное или воспалительное.
Почему применение гипсовых повязок ошибочно?
Рис. 1. Перелом эпифиза лучевой и Рис. 2. Вторичное смещение костных отломков локтевой кости.
- низкая устойчивость соединения отломков (после наложения гипсовой повязки сохраняется подвижность фрагментов до 2 град. при допустимых 0,5);
- невозможно создать компрессию (рис. 1);
- повреждение мягких тканей (пролежни, нарушение трофики);
- нарушение кровообращения в результате резкого ограничения функции поврежденной конечности;
- контрактура суставов;
- ограничение функции поврежденной конечности;
- вторичное смещение костных отломков (Рис. 2);
- отсутствие точной полной репозиции;
- несоответствие принципам функционального лечения переломов;
- атрофия мягких тканей;
- является фактором дополнительного беспокойства для животного;
- несращения, псевдоартроз.
Применение гипсовых повязок при лечении переломов противоречит принципам стабильно-функционального остеосинтеза, т.к. не обеспечивает комплекса оптимальных условий заживления перелома: нет сопоставления отломков, отсутствует высокая жесткость фиксации отломков, нарушено кровоснабжение и не сохранены функции поврежденной конечности.
Основные осложнения, с которыми приходится сталкиваться ветеринарному врачу при лечении переломов, это:
- замедленное (неполное) сращение и несрастание (Рис.3,4);
- остеомиелит;
- порочное срастание костной ткани;
- патологические процессы при переломе;
- саркома в месте перелома;
- жировая эмболия.
Рис. 3. Рис. 4.
При замедленном (неполном) сращении и несрастании необходимо понимать факторы, оказывающие влияние на время, отведенное для заживления перелома. К таким факторам относят:
- возраст (плохая минерализация, чрезмерная ломкость, плохая способность к регенерации у старых животных, «мягкие» кости у молодых);
- метод лечения (неадекватная стабилизация перелома, нарушение принципа стабильного и функционального остеосинтеза);
- тип перелома (чрезмерный дефект участка перелома: нежизнеспособный фрагмент кости, потерянный имплантат);
- поражение кости (когда имеет место инфекционный процесс); сопутствующие патологии (системные или местные болезни, идиопатические факторы).
Заключение о том, что перелом срастается медленно или не срастается вовсе, может быть сделано на основании рентгенологического исследования. Здесь можно выделить следующие особенности:
- при замедленном срастании: сохраняющаяся линия перелома при наличии признаков протекания процессов заживления; открытая мозговая полость; неровные поверхности линии перелома; отсутствие склероза.
- при несрастании: промежуток между концами сломанной кости; закрытая мозговая полость; склероз; гипертрофия или атрофия концов кости.
Несрастание перелома классифицируется по системе Вебера-Сича, описанной в 1976 г. Согласно этой классификации несрастание переломов делят на две группы: биологически активные (жизнеспособные) и биологически неактивные (нежизнеспособные). Эти две группы подразделяют на более специализированные по причине их возникновения и рентгенологическому проявлению:
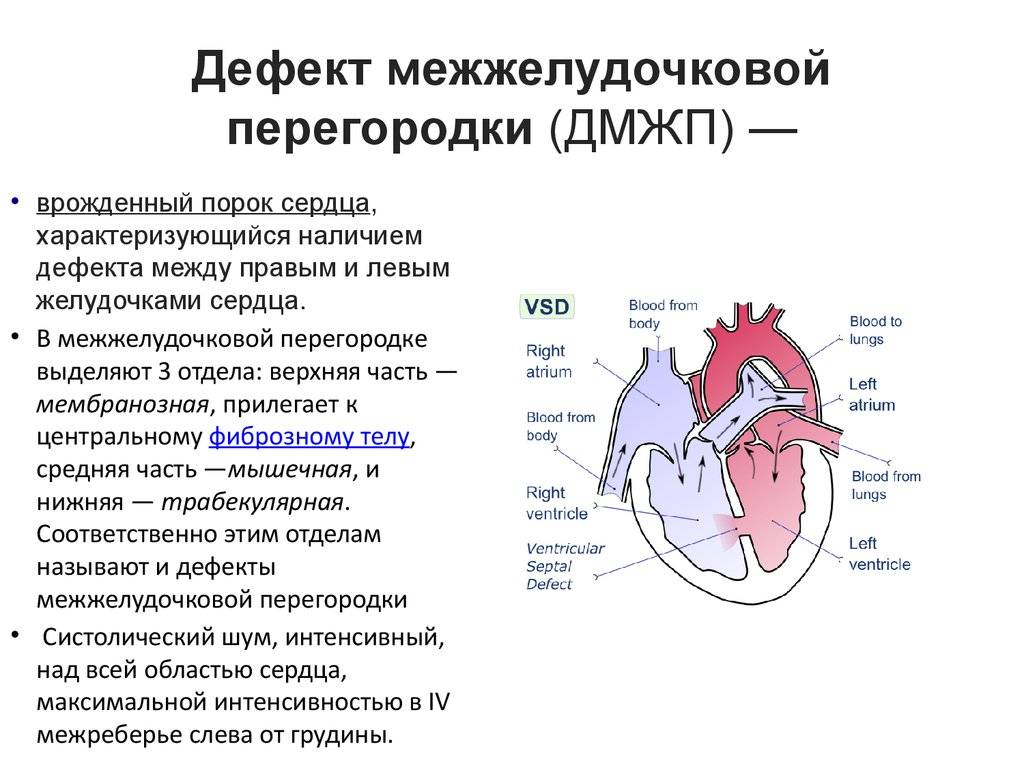
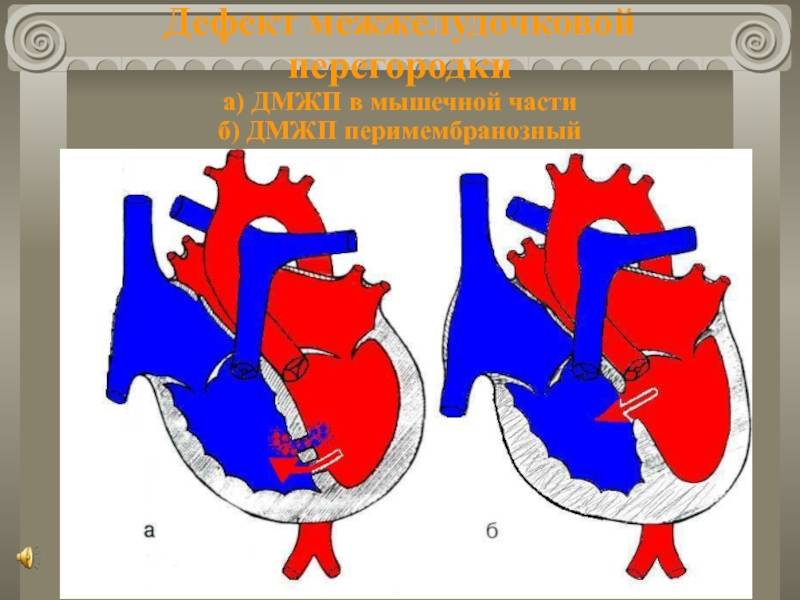
Виды дефектов межжелудочковой перегородки у новорожденных
Дефект межжелудочковой перегородки у новорожденного склонен иметь разное размещение.
Учитывая этот параметр, выделяют несколько форм болезни:
- Трабекулярный. Для него характерно размещение в любом месте мембраны, окружен мышечными волокнами.
- Перимембранозный дефект межжелудочковой перегородки у новорожденного. Чаще всего размещен книзу от аортального клапана.
- Субпульмонарный выброс. Дефект межжелудочковой перегородки сердца у новорожденных присутствует около легочной артерии. Нередко сопровождается обратным забросом аортальной крови.
- Впускная аномалия. Локализуется сзади относительно мембранной перепонки и граничит с 3-створчатым клапаном.
Если перимембранозный дефект межжелудочковой перегородки у новорожденного имеет диаметр более 1 см, развиваются осложнения — синдром Эйзенменгера, сердечная недостаточность, легочная гипертензия.
Симптоматика
Если дефекты не обладают большими размерами, то у детей они никак не проявляются. По этой причине в детском возрасте при малых отверстиях диагноз ставят редко. О проблеме узнают, когда появляются первые симптомы, а это происходит после двадцати лет.
Но если отверстие в перегородке большое, то:
- у ребенка часто возникают инфекционные болезни, которые поражают преимущественно органы дыхательной системы;
- физические нагрузки вызывают трудности с дыханием;
- повышается утомляемость, снижается работоспособность;
- кожный покров обретает бледный оттенок, а в тяжелых случаях – синеет;
- сердце сокращается нерегулярно.
Если появились такие признаки, следует провести обследование, чтобы своевременно провести хирургическое вмешательство.
Проведение диагностики
При возникновении первых признаков болезней сердца и дефекта межпредсердной перегородки нужно пройти комплексное обследование у кардиолога. Для постановки диагноза проводится комплексное обследование, позволяющее определить имеющиеся патологии в развитии сердечно-сосудистой системы и назначить соответствующее лечение. К наиболее информативным диагностическим мероприятиям можно отнести такие как:
- рентген грудной клетки;
- эхокардиография;
- кардиограмма;
- введение в сердце катетера;
- ангиокардиография.
При помощи рентгена можно определить изменение размеров сердечной мышцы и ее отдельных частей, что может говорить о наличии нарушений, а также застое крови в крупных венах. Ангиография позволяет определить наличие или отсутствие отверстий в межпредсердной перегородке. Для этого в кровь одного из предсердия вводится красящее вещество, которое обеспечивает видимость движения крови в сердце.
Все эти методы диагностики применяются к детям школьного возраста и взрослым, а у новорожденных подобная патология на протяжении длительного времени совершенно никак себя не обнаруживает. Подобное нарушение может обнаруживаться после проведения УЗИ сердца.
Для новорожденных детей применяются такие методы диагностики, как прослушивание сердца. При помощи стетоскопа доктор может обнаружить наличие посторонних шумов, что может быть при прохождении суженных клапанов в сердечной перегородке. Электрокардиография и УЗИ также позволяют определить наличие размеров сердечной мышцы и застоя крови в крупных сосудах. При наличии показаний к проведению срочного хирургического вмешательства показано проведение катетеризации сердца.
После диагностирования дефектов межпредсердной и межжелудочковой перегородки назначается соответствующее лечение, так как своевременность принимаемых мер дает возможность не только повысить качество жизни больного, но и продлить максимально период жизни.
Признаки заболевания
Если во время планового обследования в первый месяц жизни патология не выявляется, она может длительное время не проявлять себя, так как орган при данном дефекте обладает хорошими компенсаторными функциями, особенно при малых размерах ДМПП. Средние и большие просветы ведут к развитию сердечной симптоматики уже с первых дней жизни:
- посинение носогубного треугольника при плаче новорожденного;
- устойчивая бледность кожи к 3-4 месяцам жизни;
- тахикардия и незначительное отставание в физическом развитии к концу первого года;
- значительная подверженность респираторным инфекциям с одышкой и хрипами;
- в первое десятилетие появляются обмороки после физической активности, утомляемость, вертиго.
Если отверстие в перегородке не превышает нескольких миллиметров, заболевание многие годы течет бессимптомно, может проявить себя только к 20-30 годам, когда начинается постепенное развитие гипертензии легких, недостаточности сердца, аритмии, в редких случаях появляется кашель с кровавой мокротой.
Методы исследования
Заболевание может быть выявлено на плановом обследовании у кардиолога в первый год жизни ребенка. Если этого не произошло и появились явные симптомы, производится сбор анамнеза, пациент осматривается на предмет оценки цвета кожных покровов, характера дыхания, внутригрудных шумов. Далее требуется аппаратная диагностика, которая проводится следующими способами:
- ЭКГ. Показывает перегрузку в работе правосторонней части органа.
- Рентгенография. Проявляет усиленный легочный рисунок, увеличение легочной артерии и сердечной тени на снимках.
- Рентгеноскопия. Фиксирует усиление пульсации легочных корней, что является специфическим симптомом ДМПП.
- ЭхоКГ. Визуально показывает локализацию просвета, определяет его размеры, а также левосторонний сброс кровяной массы.
- Зондирование сердечных полостей. Фиксирует повышение внутрисердечного давления в правосторонних сегментах.
- МРТ сердца. Наиболее информативная методика, способная предоставить полный объем информации о состоянии сердечно-легочной системы, если остальные диагностические методики не показали эффективности.
Лучшим вариантом исследования при врожденных дефектах строения внутренних органов служит МРТ. Без травмирования и болезненности, которые присущи стандартным эндоскопическим и зондирующим методикам, без повышенного радиационного излучения в противовес рентгену, можно сделать полноценное сканирование в любом возрасте, начиная с первых дней жизни. За один короткий сеанс врачи получат исчерпывающие данные об имеющихся нарушениях, что поможет вовремя приступить к лечению, избежать тяжелых последствия в будущем.
Условия диагностики
Для томографического обследования необходимы специальные условия, которые имеются только в профильных или многофункциональных клиниках. Отыскать такие учреждения поможет наш бесплатный сервис. На сайте можно выбрать интересующую услугу, задать критерии поиска медцентра, сравнить разные варианты по ценам, расположению, рейтингам, видам оснащения, почитать отзывы и бесплатно проконсультироваться с сотрудниками службы записи по номеру на портале. Обращайтесь и бронируйте МРТ сердца удаленно со скидками от сервиса.
Лечение и прогнозы
Восстановить целостность межпредсердной перегородки можно исключительно инструментальным путем. Лучшим временем для проведения операции служит возрастной промежуток 1-12 лет. Отказаться от операции придется, если у больного выявлено чрезмерно повышенное внутрилегочное давление на фоне вено-артериального кровообращения, так как сосуды легких меньшего диаметра уже претерпевают склеротические изменения.
В хирургии используется несколько видов оперативных манипуляций:
- ушивание просвета;
- пластическое восстановление межпредсердного окна биологическим или синтетическим лоскутом;
- рентгенэндоваскулярное сужение при небольших ДМПП (до 2 см).
После проведенной манипуляции наблюдаются положительные прогнозы отдаленной перспективы в 90% случаев. Нормализация кровообращения по малому кругу наступает сразу, больные не высказывают жалоб на плохое самочувствие в связи с сердечным заболеванием. Если у человека присутствует небольшой дефект, он может вообще не проявить себя вплоть до пожилого возраста, не сопряжен с опасностями для жизни. Если обнаружено значительное изменение в строении перегородки, без лечения продолжительность жизни составляет 35-40 лет, летальный исход может наступить от дыхательных проблем или чрезмерной гипертензии.
Как все-таки вылечить пародонтоз
Информация с интернет-форумов показывает, что очень многие люди все еще путают пародонтоз с пародонтитом – воспалительным заболеванием десен. По этой причине многие описанные в интернете методики лечения пародонтоза не работают, так как на самом деле лечат пародонтит.
О пародонтозе же пользователи форумов в основном отзываются очень плохо – практически ни у кого он полностью не прошел. Многие пишут, что пародонтозом страдали их отцы или матери, и в итоге тем пришлось полностью удалять зубы и ставить протезы – только тогда заболевание, наконец, остановилось. Неплохо люди на сайтах отзываются об укрепляющих уколах, хотя есть целые группы людей, которым уколы совсем не помогают.
Многим врачи прописывают лекарства для облегчения симптомов – в виде мазей, компрессов и т.п. Курсы лечения нужно повторять регулярно, и в целом пародонтоз перестает беспокоить. Также в качестве поддержки помогают различные зубные пасты – пользователи упоминают «Лакалют», «Пародонтоцит» и «Weleda». Также хорошим дополнением будет использование ирригатора.
Пародонтоз до и после лечения
Факторы развития
Заболевание встречается, как самостоятельная патология, так и совмещенная с иными дефектами развития органа. Нарушения появляются уже в эмбриональном периоде, когда происходит формирование системы кровообращения в первом триместре беременности матери. Повлиять на естественный механизм нормального развития способны любые неблагоприятные факторы внешней и внутренней природы:
- генетическая предрасположенность, семейственность сердечных пороков, наличие старших родственников с синдромом Холта-Орама;
- вирусные болезни матери;
- эндокринные нарушения в организме женщины (особенно диабетический синдром);
- систематическое отравление плода запрещенными медикаментами, алкоголем;
- проживание и работа в экологически неблагоприятных местностях;
- повышенный радиационный фон в местах постоянного пребывания;
- осложнения беременности (угрозы прерывания, патологические токсикозы).
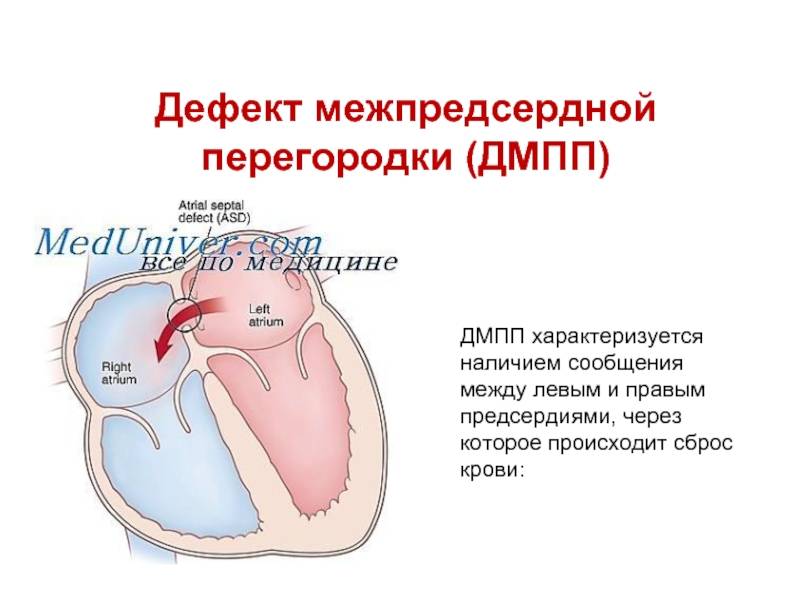
В перегородке между предсердиями может быть одно или несколько отверстий разного диаметра. От размеров просвета зависит скорость развития сердечно-легочных нарушений в работе органов, развитие дыхательной недостаточности и цианоза (посинения кожных покровов даже в состоянии покоя). Из-за неправильного распределения давления в предсердиях происходит выбухание правой стороны сердца, что приводит к сужению легочной артерии, повышению давления, дыхательной недостаточности.